题目内容
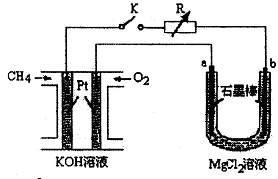
电浮选凝聚法处理酸性污水的工作原理如图。下列说法不正确的是
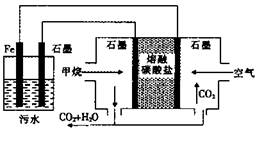

| A.铁电极的电极反应式为:Fe—2e—=Fe2+ |
| B.通人甲烷的石墨电极的电极反应式为:CH4+4CO32——8e—=5CO2+2H2O |
| C.为增强污水的导电能力,可向污水中加人适量工业用食盐 |
| D.若左池石墨电极产生44.8L气体,则消耗0. 5 mol甲烷 |
D
试题分析:A、燃料电池中通甲烷的电极为负极,通空气的电极为正极,则电解质中 Fe作阳极,阳极反应式为Fe—2e—=Fe2+,正确;B、根据电子、电荷和原子守恒可知,燃料负极反应式为CH4+4CO32——8e—=5CO2+2H2O,正确;C、食盐是电解质,加入食盐,能增大污水中离子浓度,正确;D、缺少标准状况下,不能用44.8L÷22.4L/mol求阴极产物的物质的量,也不能求转移电子的物质的量,错误。

练习册系列答案
相关题目
 从右向左移动。下列分析正确的是
从右向左移动。下列分析正确的是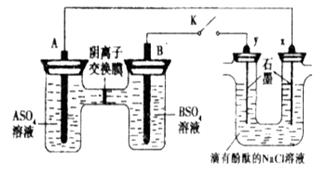
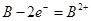
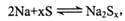 电池工作温度为320℃。下列说法错误的是
电池工作温度为320℃。下列说法错误的是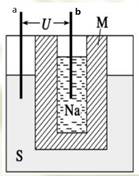
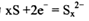
 Fe(OH)2 +2Ni(OH)2下列推断不正确的是( )
Fe(OH)2 +2Ni(OH)2下列推断不正确的是( )