题目内容
某蓄电池放电、充电时反应为:Fe+ Ni2O3 +3H2O  Fe(OH)2 +2Ni(OH)2下列推断不正确的是( )
Fe(OH)2 +2Ni(OH)2下列推断不正确的是( )
 Fe(OH)2 +2Ni(OH)2下列推断不正确的是( )
Fe(OH)2 +2Ni(OH)2下列推断不正确的是( )| A.放电时,Fe为正极,Ni2O3为负极 |
| B.充电时,阴极上的电极反应式是:Fe(OH)2 +2e-→Fe+2OH- |
| C.放电时,负极上的电极反应式是:Ni2O3 +3H2O+2e-→2Ni(HO)2 +2OH- |
| D.该蓄电池的电极必须是浸在某种碱性电解质溶液中 |
AC
试题分析:A、由放电时的反应可以得出铁做还原剂失去电子,Ni2O3做氧化剂得到电子,即正极为Ni2O3、负极为Fe,故A错误;
B、充电可以看作是放电的逆过程,即阴极为原来的负极,所以电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2,所以电池充电过程时阴极反应为Fe(OH)2+2e-=Fe+2OH-,故B正确;
C、根据总反应Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2,可以判断出铁镍蓄电池放电时Fe作负极,发生氧化反应,为还原剂,失电子生成Fe2+,碱性电解质中最终生成Fe(OH)2,负极反应为:Fe+2OH--2e-=Fe(OH)2,Ni2O3+3H2O+2e-→2Ni(HO)2+2OH-为正极反应,故C错误;
D、Fe(OH)2、2Ni(OH)2只能存在于碱性溶液中,在酸性条件下不能存在,故D正确.
故选AC.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 Li2SO4 + Al2O3·4SiO2·H2O↓
Li2SO4 + Al2O3·4SiO2·H2O↓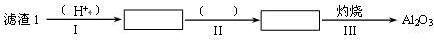
 Li1-xCoO2+LixC6。下列说法正确的是
Li1-xCoO2+LixC6。下列说法正确的是
 MnO2+Zn+2H2SO4
MnO2+Zn+2H2SO4