题目内容
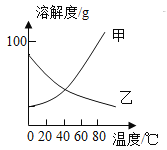
【题目】甲、乙两种固体纯净物的溶解度曲线如图所示。在常温下,先在两支试管里分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里。下列说法正确的是( )
A. 乙溶液中溶质的质量分数增大
B. 装甲溶液的试管中剩余的固体减少
C. 试管里甲、乙物质的溶解度都增大
D. 两支试管里剩余的固体都增多
【答案】A
【解析】
常温下物质的饱和溶液(试管底部均有未溶解的固体)放进盛有冰水的烧杯里,目的是对饱和溶液进行降温;根据溶解度曲线得知,甲物质的溶解度随温度降低而减小,乙物质的溶解度随温度降低而增大,据此分析解答。
A.乙物质的溶解度随温度降低变大,所以放入冰水后,随温度降低,试管底部固体物质乙继续溶解,溶液中溶质质量增加,所以乙溶液中溶质的质量分数增大,故A正确;
B.根据甲物质的溶解度曲线,温度降低,甲物质的溶解度减小,所以,放入冰水后,随温度降低,试管内饱和溶液析出晶体,剩余固体物质甲增加,故B错误;
C.固体物质的溶解度受温度影响,根据溶解度曲线,甲物质的溶解度随温度降低而减小,乙物质的溶解度随温度降低而增大,故C错误;
D.综合A、B两项的分析,盛甲物质的试管内固体物质增加,盛乙物质的试管内固体物质减少,故D错误;
故选A。

练习册系列答案
相关题目