题目内容
【题目】根据下列信息判断氢气燃烧生成水时的热量变化,下列说法正确的是( )
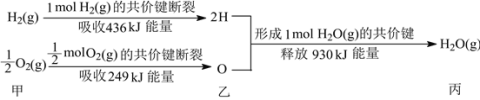
A.H2(g)与O2(g)反应生成1molH2O(g)时放出热量930kJ
B.H2O(g)分解为H2(g)与O2(g)时放出热量
C.图中甲、乙、丙中物质所具有的总能量大小关系为:乙>甲>丙
D.1molH2(g)和![]() molO2(g)的总能量小于1molH2O(g)的能量
molO2(g)的总能量小于1molH2O(g)的能量
【答案】C
【解析】
A.H2(g)与O2(g)反应生成1molH2O(g)时放出热量930kJ-436kJ-249kJ=245kJ,A不正确;
B.H2(g)与O2(g)反应生成H2O(g)时放出热量,则H2O(g)分解为H2(g)与O2(g)时吸收热量,B不正确;
C.物质具有的键能越大,则其所具有的能量越低,由图中甲、乙、丙三种物质的键能,可确定三种物质所具有的总能量大小关系为:乙>甲>丙,C正确;
D.因为H2(g)与O2(g)反应生成1molH2O(g)时放热,所以1molH2(g)和![]() molO2(g)的总能量大于1molH2O(g)的能量,D不正确;
molO2(g)的总能量大于1molH2O(g)的能量,D不正确;
故选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】乙二酸俗称草酸,是一种二元弱酸(结构简式为HOOC﹣COOH,可简写为H2C2O4),它是一种重要的化工原料。(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示)填空:
H2C2O4 | KHC2O4 | K2C2O4 | |
pH | 2.1 | 3.1 | 8.1 |
(1)写出H2C2O4的电离方程式_____________
(2)KHC2O4溶液显酸性的原因是___________
(3)向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是________。
A.c(K+)═ c(HC2O4﹣)+c(H2C2O4)+c(C2O42﹣)
B.c(Na+)═ c(H2C2O4)+c(C2O42﹣)
C.c(K+)+c(Na+)═ c(HC2O4﹣)+c(C2O42﹣)
D.c(K+)>c(Na+)