题目内容
二氧化碳、氢气、一氧化碳组成的混合气体在同温、同压下与氮气的密度相同。则该混合气体中二氧化碳、氢气、一氧化碳的体积比为( )
| A.29:8:13 | B.22:1:14 | C.13:8:13 | D.26:12:14 |
C
解析试题分析:同温同压下,气体的密度比等于摩尔质量比,所以CO2、H2、CO组成的混合气体的平均摩尔质量等于N2的摩尔质量即28 g·mol–1,而CO的摩尔质量为28g·mol–1,则只要CO2和H2的平均摩尔质量为28g·mol–1即可满足题目要求。设CO2的物质的量为x,H2的物质的量为y,则: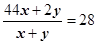 ,求得x:y=13:8,同温同压下,气体的体积之比等于物质的量之比,所以,只要满足CO2与H2的体积之比等于13:8,CO为任意值都可。故选C。
,求得x:y=13:8,同温同压下,气体的体积之比等于物质的量之比,所以,只要满足CO2与H2的体积之比等于13:8,CO为任意值都可。故选C。
考点:考查阿伏伽德罗定律及推论、混合物的有关计算。

 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案下列叙述中错误的是
| A.相同体积的任何气体都含有相同数目的原子 |
| B.标准状况下,5L H2S气体与5L NH3的原子个数比为3∶4 |
| C.同温同压下相同体积的N2气和CO气体有相同物质的量和相同的质量 |
| D.当粒子数相同时,气体的体积主要决定于气体粒子之间的距离 |
有五瓶溶液分别是:①10mL 0.60moL·L-1NaOH溶液 ②20mL 10.50moL·L-1H2SO4溶液 ③30mL0.40moL·L-1HCl溶液 ④40mL0.30moL·L-1CH3COOH溶液 ⑤50mL
0.20moL·L-1蔗糖水溶液。以上各瓶溶液所含离子、分子总数的大小顺序是
| A.⑤>④>③>②>① | B.②>①>③>④>⑤ |
| C.②>③>④>①>⑤ | D.①>②>③>④>⑤ |
硫酸铜水溶液呈酸性,属保护性无机杀菌剂,对人畜比较安全,其与石灰乳混合可得“波尔多液”。实验室里需用180mL0.10mol·L-1的硫酸铜溶液,则应选用的容量瓶规格和称取溶质的质量分别为
| A.180mL容量瓶,称取2.88g硫酸铜 |
| B.200mL容量瓶,称取5.00g胆矾 |
| C.250mL容量瓶,称取6.25g胆矾 |
| D.250mL容量瓶,称取4.0g硫酸铜 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,22.4LCCl4含有C-Cl键的数目为4NA |
| B.常温常压下,44 g由N2O与CO2组成的混合气体含有的氧原子数目为NA |
C.反应NH4N3 2N2↑+2H2↑,常温常压下每生成22.4LlN2,转移电子的数目为4NA 2N2↑+2H2↑,常温常压下每生成22.4LlN2,转移电子的数目为4NA |
| D.1 L 1 mol·L-1的AlCl3溶液中含有Cl-的数目为3NA |
用已准确称量过的氯化钠固体配制2.00mol·L-1的NaCl溶液0.2L,需要用到的仪器是:
①坩埚②分液漏斗③容量瓶④烧杯⑤胶头滴管⑥烧瓶⑦玻璃棒⑧托盘天平⑨药匙
| A.③④⑤⑦⑨ | B.①②⑤⑥⑧ | C.③④⑤⑦ | D.③④⑤⑥ |
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A.标准状况下,22.4LH2O含有的分子数为 NA |
| B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C.通常状况下,NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为 NA |
在NaCl、MgCl2两种盐配制的混合液中,Na+为0.2 mol,Mg2+为0.25 mol,
则Cl-为
| A.0.5 mol | B.0.6 mol | C.0.7 mol | D.0.8 mol |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.2.3g金属钠与过量的氧气反应,无论是否加热与否转移电子数均为0.1NA |
| B.1mol Na2CO3晶体中含CO32-离子数小于NA |
| C.惰性电极电解食盐水,若线路中通过NA个电子,则阳极产生气体11.2L |
| D.0.1mol的CaO2中含阴离子数是0.2 NA |