题目内容
用已准确称量过的氯化钠固体配制2.00mol·L-1的NaCl溶液0.2L,需要用到的仪器是:
①坩埚②分液漏斗③容量瓶④烧杯⑤胶头滴管⑥烧瓶⑦玻璃棒⑧托盘天平⑨药匙
| A.③④⑤⑦⑨ | B.①②⑤⑥⑧ | C.③④⑤⑦ | D.③④⑤⑥ |
C
解析试题分析:准确配制一定体积、一定浓度的溶液,在已准确称量后还需要用烧杯溶解,用玻璃棒搅拌、引流,用胶头滴管定容,用容量瓶盛装溶液。选项为:C。
考点:考查准确配制一定体积、一定物质的量浓度的溶液需要用到的仪器等相关知识。

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
下列化学用语正确的是( )
A.CO2的电子式: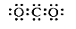 |
B.次氯酸的电子式: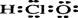 |
C.CH4分子的比例模型: |
D.Cl-的结构示意图: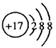 |
20℃时,饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中不正确的是
| A.20℃时,饱和KCl溶液与等质量的水混合后物质的量浓度大于2.0 mol·L-1 |
| B.20℃时,将29.8 gKCl溶于87.6 g水中可得饱和溶液 |
| C.20℃时,密度小于1.174 g·cm-3的KCl溶液是不饱和溶液 |
| D.将此溶液蒸发部分水,再恢复到20℃时,溶液中各离子的浓度不变 |
标准状况下H2和Cl2组成的混合气体2.24L,经点燃充分反应后,缓缓通入100mL 1.2mol/LNaOH溶液中恰好完全反应,测得最终溶液中NaClO的浓度为0.2mol/L(假设溶液体积不变),则原混合气体中Cl2的体积分数(物质的量百分含量)为
| A.55% | B.60% | C.65% | D.70% |
二氧化碳、氢气、一氧化碳组成的混合气体在同温、同压下与氮气的密度相同。则该混合气体中二氧化碳、氢气、一氧化碳的体积比为( )
| A.29:8:13 | B.22:1:14 | C.13:8:13 | D.26:12:14 |
质量相同的Na、Mg、Al、Zn分别放入足量的稀盐酸中,在相同的条件下,产生氢气最多的是
| A.Na | B.Mg | C.Al | D.Zn |
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.28g氮气所含有的原子数目为NA |
| B.1mol铁与足量稀盐酸反应转移的电子数目为3NA |
| C.标准状况下,22.4L水中含有的水分子数目为NA |
| D.10g重水(2H216O)中含有的中子数目为5NA |
下列有关“规定”正确的是
| A.PH小于7的雨水称为酸雨 |
| B.空气中直径大于2.5μm的颗粒物称为PM2.5 |
| C.分散质粒子直径介于1nm~100nm之间的分散系称为胶体 |
| D.标况下的气体摩尔体积为22.4L |
把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡;另一份加入含b mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁。则原混合溶液中钾离子的浓度为
A.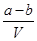 mol·L-1 mol·L-1 | B.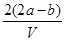 mol·L-1 mol·L-1 |
C.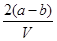 mol·L-1 mol·L-1 | D.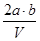 mol·L-1 mol·L-1 |