题目内容
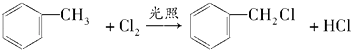
【题目】已知:①RNH2+R′CH2Cl ![]() RNHCH2R′+HCl(R和R′代表烃基) ②苯的同系物能被高锰酸钾氧化,如:
RNHCH2R′+HCl(R和R′代表烃基) ②苯的同系物能被高锰酸钾氧化,如: ![]()
![]()
![]()
③ ![]()
![]()
![]() (苯胺,弱碱性,易被氧化)化合物C是制取消炎灵(祛炎痛)的中间产物,其合成路线如图所示:
(苯胺,弱碱性,易被氧化)化合物C是制取消炎灵(祛炎痛)的中间产物,其合成路线如图所示: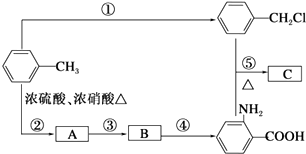
请回答下列问题:
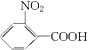
(1)B物质的结构简式是 .
(2)写出反应①、②的化学方程式: ①;
② .
(3)反应①~⑤中,属于取代反应的是(填反应序号).
【答案】
(1)
(2) ;
;
(3)①②⑤
【解析】解:甲苯在光照条件发生甲基上取代反应生成 ![]() ,由A系列反应得到
,由A系列反应得到 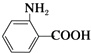 ,反应中引入﹣COOH、﹣NH2 , 且处于邻位,甲基氧化得到﹣COOH,由题目信息可知,﹣NO2还原得到﹣NH2 , 由于苯胺易被氧化,所以用KMnO4(H+)先氧化﹣CH3成﹣COOH,再将﹣NO2还原得到﹣NH2 , 故A转化得到B是甲苯的硝化反应,可知A为
,反应中引入﹣COOH、﹣NH2 , 且处于邻位,甲基氧化得到﹣COOH,由题目信息可知,﹣NO2还原得到﹣NH2 , 由于苯胺易被氧化,所以用KMnO4(H+)先氧化﹣CH3成﹣COOH,再将﹣NO2还原得到﹣NH2 , 故A转化得到B是甲苯的硝化反应,可知A为 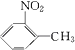 ,B为
,B为 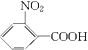 ,
, 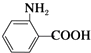 和
和 ![]() 发生取代反应生成C,由信息(1)可知生成C为
发生取代反应生成C,由信息(1)可知生成C为 ![]() .(1)B物质的结构简式是
.(1)B物质的结构简式是  ,故答案为:
,故答案为:  ;(2)反应①的化学方程式为:
;(2)反应①的化学方程式为: 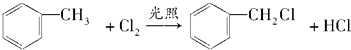 ;反应②的化学方程式为:
;反应②的化学方程式为:  ,
,
故答案为:  ;
;  ;(3)反应①~⑤中,①②⑤属于取代反应,反应③属于氧化反应,反应④属于还原反应,
;(3)反应①~⑤中,①②⑤属于取代反应,反应③属于氧化反应,反应④属于还原反应,
故答案为:①②⑤.
甲苯在光照条件发生甲基上取代反应生成 ![]() ,由A系列反应得到
,由A系列反应得到  ,反应中引入﹣COOH、﹣NH2 , 且处于邻位,甲基氧化得到﹣COOH,由题目信息可知,﹣NO2还原得到﹣NH2 , 由于苯胺易被氧化,所以用KMnO4(H+)先氧化﹣CH3成﹣COOH,再将﹣NO2还原得到﹣NH2 , 故A转化得到B是甲苯的硝化反应,可知A为
,反应中引入﹣COOH、﹣NH2 , 且处于邻位,甲基氧化得到﹣COOH,由题目信息可知,﹣NO2还原得到﹣NH2 , 由于苯胺易被氧化,所以用KMnO4(H+)先氧化﹣CH3成﹣COOH,再将﹣NO2还原得到﹣NH2 , 故A转化得到B是甲苯的硝化反应,可知A为 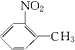 ,B为
,B为 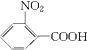 ,
,  和
和 ![]() 发生取代反应生成C,由信息(1)可知生成C为
发生取代反应生成C,由信息(1)可知生成C为 ![]() ,据此进行解答.
,据此进行解答.

【题目】一定温度下,在三个体积均为2.5L的恒容密闭容器中发生反应:CO2(g)+H2S(g)COS(g)+H2O(g)
容器 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 | |
CO2 | H2S | H2O | |||
Ⅰ | 607 | 0.11 | 0.41 | 0.01 | / |
Ⅱ | 607 | 0.22 | 0.82 | / | |
Ⅲ | 620 | 0.1 | 0.4 | / | 6.74×10﹣3 |
下列说法正确的是( )
A.该反应正反应为放热反应
B.607K时该反应的平衡常数为2.50×10﹣3
C.容器Ⅱ达到平衡时容器中COS的物质的量为0.02mol
D.容器Ⅲ达平衡时,再充入少量氦气,平衡将向正反应方向移动


