题目内容
3.除了酸以外,某些盐也能溶解沉淀.利用下表三种试剂进行实验,相关分析不正确的是( )| 编号 | ① | ② | ③ |
| 分散质 | Mg(OH)2 | HCl | NH4Cl |
| 备注 | 悬浊液 | 1mol/L | 1mol/L |
| A. | 向①中加入②,c(OH-)减小,Mg(OH)2溶解平衡正向移动 | |
| B. | 向①中加入酚酞显红色,说明物质的“不溶性”是相对的 | |
| C. | 向①中加入③,沉淀溶解,说明Mg(OH)2比NH3•H2O更难电离 | |
| D. | ①③混合后发生反应:Mg(OH)2(s)+2NH4+?Mg2++2NH3•H2O |
分析 A.根据Mg(OH)2的沉淀溶解平衡移动分析;
B.Mg (OH)2是难溶电解质,没有绝对不溶的物质;
C.醋酸铵电离生成的铵根离子和氢氧根离子反应生成一水合氨,促进氢氧化镁溶解;
D.NH4+能结合Mg(OH)2电离的氢氧根离子,生成弱电解质.
解答 解:A.在Mg(OH)2的悬浊液中存在沉淀溶解平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),所以向①中加入②,c(OH-)减小,Mg(0H)2溶解平衡正向移动,故A正确;
B.Mg (OH)2是难溶电解质,在水中有少量的溶解,而且电离出氢氧根离子,溶液显弱碱性,所以没有绝对不溶的物质,故B正确;
C.醋酸铵电离生成的铵根离子和氢氧根离子反应生成一水合氨,从而使Mg(OH)2 ?Mg2++2OH-平衡向右移动,说明NH3•H2O比Mg(OH)2更难电离,故C错误;
D.NH4+能结合Mg(OH)2电离的氢氧根离子,生成弱电解质NH3•H2O,所以①、③混合后发生反应:Mg(OH)2(s)+2NH4+?Mg2++2NH3•H2O,故D正确.
故选C.
点评 本题考查了难容电解质的溶解平衡,注意从平衡移动的角度分析沉淀的溶解和转化,题目难度不大.

练习册系列答案
相关题目
13.石油被称为工业的血液,煤被称为工业的粮食.下列说法正确的是( )
| A. | 煤的干馏产物全部是有机物 | |
| B. | 石油的分馏、煤的干馏都属于化学变化 | |
| C. | 煤焦油经过分馏可以得到苯、甲苯等,说明煤中含有苯和甲苯 | |
| D. | 石油的裂化、裂解说明烃在加热条件下是可以分解的 |
18.分别在250℃和T℃下将1mol CO和2molH2充入一容积为1L的密闭容器中发生反应:CO(g)+2H2(g)?CH2OH(g)△H=a kJ/mol,结合如图分析下列说法中正确的是( )

| A. | 混合气体的密度不变能说明该反应到达平衡状态 | |
| B. | a>0 | |
| C. | 其他条件不变,若减小容积体积,CO质量分数增大 | |
| D. | 平衡常数K:T℃时大于250℃ |
8.下列离子方程式书写不正确的是( )
| A. | FeO溶于稀硝酸:FeO+2H+═Fe2++H2O | |
| B. | 醋酸与碳酸钙反应:2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2↑ | |
| C. | Ba(OH)2溶液与稀硫酸反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 往AlC13溶液中加入过量氨水:Al3++3 NH3•H2O═Al(OH)3↓+3NH4+ |
15.2012年诺贝尔化学奖获得者利用${\;}_{53}^{151}$I研究G蛋白偶联受体,下列说法正确的是( )
| A. | I元素的质量数是131 | B. | I元素的中子数是78 | ||
| C. | I原子5p亚层有一个未成对电子 | D. | I原子有53个能量不同的电子 |
12. 我国科研人员以蹄叶橐吾为原料先制得化合物Ⅰ,再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法不正确的是( )
我国科研人员以蹄叶橐吾为原料先制得化合物Ⅰ,再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法不正确的是( )
 我国科研人员以蹄叶橐吾为原料先制得化合物Ⅰ,再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法不正确的是( )
我国科研人员以蹄叶橐吾为原料先制得化合物Ⅰ,再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法不正确的是( )| A. | 化合物Ⅰ能使酸性高锰酸钾溶液褪色 | |
| B. | 化合物Ⅰ分子中含有5个手性碳原4 | |
| C. | 化合物Ⅱ一定条件下能发生取代、消去及加成反应 | |
| D. | 检验化合物Ⅱ是否含化合I可用Br2的CCl4溶液 |
13.两种金属混合物共15g,投入足量的盐酸中,充分反应后得到11.2L H2(标准状况),则原混合物的组成肯定不可能为( )
| A. | Mg和Al | B. | Zn和Cu | C. | Al和Zn | D. | Al和Cu |
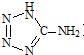 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.