题目内容
13.两种金属混合物共15g,投入足量的盐酸中,充分反应后得到11.2L H2(标准状况),则原混合物的组成肯定不可能为( )| A. | Mg和Al | B. | Zn和Cu | C. | Al和Zn | D. | Al和Cu |
分析 假设金属均为+2价,金属总物质的量等于氢气物质的量,根据n=$\frac{m}{M}$计算混合金属平均摩尔质量;因为为两种金属的混合物,故平均摩尔质量应介于各组分之间,根据电子转移守恒,若金属不与盐酸反应,其摩尔质量可以视作无穷大;Al为+2价时的摩尔质量为:$\frac{27g/mol}{3}$×2=18g/mol,据此进行解答.
解答 解:标况下11.2L氢气物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,
假设金属均为+2价,金属总物质的量等于氢气物质的量,
故混合金属平均摩尔质量为:$\frac{15g}{0.5mol}$=30g/mol,因为为两种金属的混合物,故该平均摩尔质量应介于各组分之间,
A.Mg的摩尔质量为24g/mol,Al为+2价时的摩尔质量为:$\frac{27g/mol}{3}$×2=18g/mol,二者的摩尔质量都小于30g/mol,不可能为二者的组合,故A正确;
B.Cu不与盐酸反应,其摩尔质量可以视作无穷大;锌的摩尔质量为65g/mol,二者的摩尔质量都大于30g/mol,不可能为二者的组合,故B正确;
C.Al为+2价时的摩尔质量为:$\frac{27g/mol}{3}$×2=18g/mol,锌的摩尔质量为65g/mol,二者的平均摩尔质量可以为30g/mol,故C错误;
D.Cu不与盐酸反应,其摩尔质量可以视作无穷大,Al为+2价时的摩尔质量为:$\frac{27g/mol}{3}$×2=18g/mol,可以为二者的组合,故D错误;
故选AB.
点评 本题考查混合物反应的计算,题目难度中等,注意明确金属与酸反应的实质,熟练掌握平均摩尔质量在化学计算中的应用方法,试题充分考查了学生的分析、理解能力及化学计算能力.

| 编号 | ① | ② | ③ |
| 分散质 | Mg(OH)2 | HCl | NH4Cl |
| 备注 | 悬浊液 | 1mol/L | 1mol/L |
| A. | 向①中加入②,c(OH-)减小,Mg(OH)2溶解平衡正向移动 | |
| B. | 向①中加入酚酞显红色,说明物质的“不溶性”是相对的 | |
| C. | 向①中加入③,沉淀溶解,说明Mg(OH)2比NH3•H2O更难电离 | |
| D. | ①③混合后发生反应:Mg(OH)2(s)+2NH4+?Mg2++2NH3•H2O |
| 化合物 | A | B | C |
| 结构简式 | 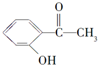 | 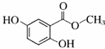 | 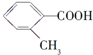 |
| 化合物 | D | E | F |
| 结构简式 |  | 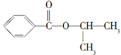 |  |
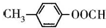 .
.A.核磁共振氢谱有4组峰
B.能发生水解反应
C.在加热条件下能够与新制的氢氧化铜悬浊液生成砖红色沉淀
(2)化合物B是制取抗心律失常药物--氟卡尼的中间体,下列有关描述不正确的是BD(填字母).
A.能与氯化铁溶液显色 B.分子中含有羧基、羟基等官能团
C.能与溴水反应 D.能与碳酸钠溶液反应产生二氧化碳
(3)化合物B在一定条件下,可以与NaOH溶液发生反应,则1mol化合物B最多需要NaOH的物质的量为3mol.
(4)化合物C与D在一定条件下发生如下转化得到高分子化合物Z,部分产物已略去.
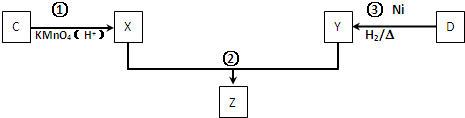
反应③中D与H2按物质的量1:1反应生成Y,则反应②的化学方程式为
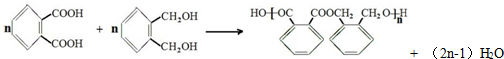 .
.(5)化合物D与银氨溶液反应的化学方程式(有机物用结构简式表示):
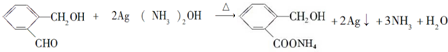 .
.(6)化合物F是合成克矽平的原料之一,(克矽平是一种治疗矽肺病的药物),其合成路线如下(反应均在一定条件下进行):
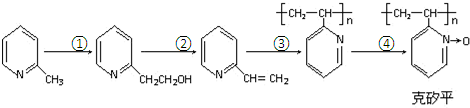
a.反应①是原子利用率100%的反应,则该反应的化学方程式为
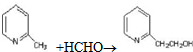 ;
;b.上述转化关系中没有涉及的反应类型是③⑥(填代号).
①加成反应 ②消去反应 ③还原反应 ④氧化反应 ⑤加聚反应 ⑥取代反应.
| A. | 1mol氯气 | B. | 1mol S | ||
| C. | 含1molHNO3的稀硝酸 | D. | 含1molCuSO4的硫酸铜溶液 |
| A. | 在Fe2(SO4)3溶液中加入过量的铁粉,过滤,在滤液中加入过量的NaOH溶液 | |
| B. | 用铁粉与稀硫酸充分反应,然后再加入过量的氨水 | |
| C. | 在FeCl2溶液上加一层苯,然后将滴管插入到FeCl2溶液液面以下,慢慢滴加NaOH溶液(溶液中不能有气泡,配制FeCl2和NaOH溶液的蒸馏水必须加热煮沸) | |
| D. | 在生成Fe(OH)3的悬浊液中加过量的铁粉 |

| 实验一 | 实验二 | |
| 实验药品 | 4g P2O5、8mL无水乙醇 | |
| 实验条件 | 酒精灯加热 | 水浴加热 |
实验现象 | 无水乙醇加入时,圆底烧瓶B中P2O5溶于乙醇,立即产生白雾,当用酒精灯加热后,有气泡产生,并逐渐沸腾,生成粘稠状液体,集气瓶C中有无色液体产生. | 无水乙醇加入时,圆底烧瓶B中P2O5溶于乙醇立即产生白雾,当用水浴加热后,无气泡产生,生成粘稠状液体,集气瓶C中有无色液体产生. |
(1)写出装置中仪器A的名称分液漏斗;
(2)装置中B、C之间长导管的作用是导气、冷凝,浓硫酸的作用是干燥气体;
(3)实验二中,完成水浴加热必需的玻璃仪器有大烧杯、酒精灯;
(4)实验一、二中当加入无水乙醇时,均有白雾产生,请简述产生白雾的原因:P2O5溶解于乙醇,迅速放出大量的热,局部温度较高,使得少量乙醇气化,形成白雾;
(5)经检验集气瓶C中无色液体为磷酸三乙酯,请在图中虚线框内画出实验装置(含试剂)用于验证生成的乙烯;
(6)根据实验现象判断以P2O5作为催化剂获得乙烯的反应条件是加热至较高温度.
| A. | 氨水 | B. | SO2 | C. | CH3COOH | D. | BaSO4 |
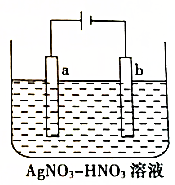 如图为电解精炼银的示意图,a(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为NO3-+e-+2H+=NO2↑+H2O.
如图为电解精炼银的示意图,a(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为NO3-+e-+2H+=NO2↑+H2O.