题目内容
15.2012年诺贝尔化学奖获得者利用${\;}_{53}^{151}$I研究G蛋白偶联受体,下列说法正确的是( )| A. | I元素的质量数是131 | B. | I元素的中子数是78 | ||
| C. | I原子5p亚层有一个未成对电子 | D. | I原子有53个能量不同的电子 |
分析 元素符号的左上角表示质量数,左下角表示质子数,质子数=核电荷数=核外电子数,质量数=质子数+中子数,利用此知识解决即可.
解答 解:已知13153I,则该元素:质子数=核电荷数=核外电子数=53;质量数为131,则中子数=131-53=78
A.${\;}_{53}^{151}$I的质量数是151,不是碘元素的质量数,故A错误;
B.${\;}_{53}^{151}$I的中子数是78,不是碘元素的中子数,故B错误;
C.碘原子的5p亚层有5个电子,则有4个成对电子,有一个未成对电子,故C正确;
D.I外围电子排布为5s25p5,处于第五周期ⅦA族,有1s、2s、2p、3s、3p、3d、4s、4p、4d、5s、5p共10种不同能量的电子,故D错误.
故选C.
点评 本题主要考查了原子符号的含义,难度不大,明确在原子中:质子数=电子数=核电荷数;相对原子质量=质子数+中子数是解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
5.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g);△H=+49.0kJ/mol
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g);△H=-192.9kJ/mol
下列说法正确的是( )
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g);△H=+49.0kJ/mol
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g);△H=-192.9kJ/mol
下列说法正确的是( )
| A. | CH3OH的燃烧为吸热反应 | |
| B. | 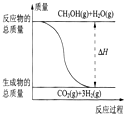 反应①中的能量变化如图所示 | |
| C. | CH3OH转变成H2的过程一定要吸收能量 | |
| D. | 根据②推知反应:CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)的△H>-192.9kJ/mol |
3.除了酸以外,某些盐也能溶解沉淀.利用下表三种试剂进行实验,相关分析不正确的是( )
| 编号 | ① | ② | ③ |
| 分散质 | Mg(OH)2 | HCl | NH4Cl |
| 备注 | 悬浊液 | 1mol/L | 1mol/L |
| A. | 向①中加入②,c(OH-)减小,Mg(OH)2溶解平衡正向移动 | |
| B. | 向①中加入酚酞显红色,说明物质的“不溶性”是相对的 | |
| C. | 向①中加入③,沉淀溶解,说明Mg(OH)2比NH3•H2O更难电离 | |
| D. | ①③混合后发生反应:Mg(OH)2(s)+2NH4+?Mg2++2NH3•H2O |
20.某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )
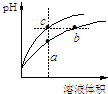

| A. | a、c两点溶液的导电能力相同 | |
| B. | b点溶液中c(H+)+c(NH3•H2O)=c(OH-) | |
| C. | a、b、c三点溶液水的电离程度a>b>c | |
| D. | 与等体积b、c处溶液反应,消耗等量的NaOH |
4.已知A--F六种有机化合物是重要的有机合成原料,结构简式见下表,请根据要求回答下列问题:
(1)写出符合下列条件的A的同分异构体的结构简式: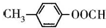 .
.
A.核磁共振氢谱有4组峰
B.能发生水解反应
C.在加热条件下能够与新制的氢氧化铜悬浊液生成砖红色沉淀
(2)化合物B是制取抗心律失常药物--氟卡尼的中间体,下列有关描述不正确的是BD(填字母).
A.能与氯化铁溶液显色 B.分子中含有羧基、羟基等官能团
C.能与溴水反应 D.能与碳酸钠溶液反应产生二氧化碳
(3)化合物B在一定条件下,可以与NaOH溶液发生反应,则1mol化合物B最多需要NaOH的物质的量为3mol.
(4)化合物C与D在一定条件下发生如下转化得到高分子化合物Z,部分产物已略去.
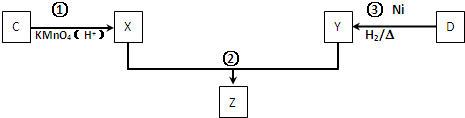
反应③中D与H2按物质的量1:1反应生成Y,则反应②的化学方程式为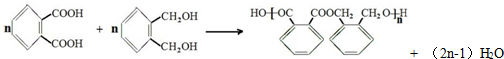 .
.
(5)化合物D与银氨溶液反应的化学方程式(有机物用结构简式表示):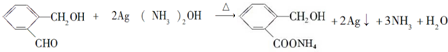 .
.
(6)化合物F是合成克矽平的原料之一,(克矽平是一种治疗矽肺病的药物),其合成路线如下(反应均在一定条件下进行):
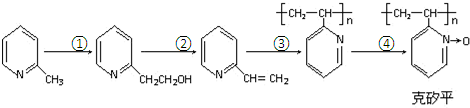
a.反应①是原子利用率100%的反应,则该反应的化学方程式为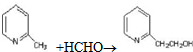 ;
;
b.上述转化关系中没有涉及的反应类型是③⑥(填代号).
①加成反应 ②消去反应 ③还原反应 ④氧化反应 ⑤加聚反应 ⑥取代反应.
| 化合物 | A | B | C |
| 结构简式 | 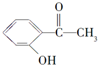 | 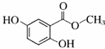 | 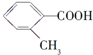 |
| 化合物 | D | E | F |
| 结构简式 |  | 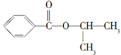 |  |
 .
.A.核磁共振氢谱有4组峰
B.能发生水解反应
C.在加热条件下能够与新制的氢氧化铜悬浊液生成砖红色沉淀
(2)化合物B是制取抗心律失常药物--氟卡尼的中间体,下列有关描述不正确的是BD(填字母).
A.能与氯化铁溶液显色 B.分子中含有羧基、羟基等官能团
C.能与溴水反应 D.能与碳酸钠溶液反应产生二氧化碳
(3)化合物B在一定条件下,可以与NaOH溶液发生反应,则1mol化合物B最多需要NaOH的物质的量为3mol.
(4)化合物C与D在一定条件下发生如下转化得到高分子化合物Z,部分产物已略去.

反应③中D与H2按物质的量1:1反应生成Y,则反应②的化学方程式为
 .
.(5)化合物D与银氨溶液反应的化学方程式(有机物用结构简式表示):
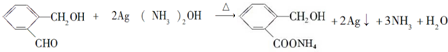 .
.(6)化合物F是合成克矽平的原料之一,(克矽平是一种治疗矽肺病的药物),其合成路线如下(反应均在一定条件下进行):

a.反应①是原子利用率100%的反应,则该反应的化学方程式为
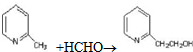 ;
;b.上述转化关系中没有涉及的反应类型是③⑥(填代号).
①加成反应 ②消去反应 ③还原反应 ④氧化反应 ⑤加聚反应 ⑥取代反应.
5.下列实验方案可以得到白色纯净的Fe(OH)2的是( )
| A. | 在Fe2(SO4)3溶液中加入过量的铁粉,过滤,在滤液中加入过量的NaOH溶液 | |
| B. | 用铁粉与稀硫酸充分反应,然后再加入过量的氨水 | |
| C. | 在FeCl2溶液上加一层苯,然后将滴管插入到FeCl2溶液液面以下,慢慢滴加NaOH溶液(溶液中不能有气泡,配制FeCl2和NaOH溶液的蒸馏水必须加热煮沸) | |
| D. | 在生成Fe(OH)3的悬浊液中加过量的铁粉 |
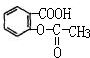 它的化学式为C9H8O4,其分子中含有羧基和酯基两种官能团(写官能团的名称),下列反应能发生的是(填字母):A、B、D(选项:A取代反应、B水解反应、C消去反应、D加成反应),该化合物1mol最多能跟3molNaOH反应.
它的化学式为C9H8O4,其分子中含有羧基和酯基两种官能团(写官能团的名称),下列反应能发生的是(填字母):A、B、D(选项:A取代反应、B水解反应、C消去反应、D加成反应),该化合物1mol最多能跟3molNaOH反应. .
.