��Ŀ����
������Ũ��Ϊ0.01 mol / L������һԪ����Һ��HA��HB��HC������HA��c(H+)��0.001 mol / L��HB�ĵ����Ϊ0.1%��HC��c(OH��)��1��10��12mol / L�������������������γɵ����Σ�NaA��NaB��NaC����Һ�����ʵ���Ũ����ͬ������£���pHֵ�ɴ�С��˳���ǣ���
A��NaA��NaB��NaC B��NaB��NaA��NaC
C��NaB��NaC��NaA D��NaC��NaA��NaB
A��NaA��NaB��NaC B��NaB��NaA��NaC
C��NaB��NaC��NaA D��NaC��NaA��NaB
B
������֪HA�ĵ����ҲΪ10% ��H C��Һ��c(H+)��1��10��2mol / L����ȫ�����룬Ϊǿ�ᡣ�ɡ�Խ��Խˮ�⡱֪���������γɵ����Σ�pHֵ�ɴ�С��˳����NaB��NaA��NaC

��ϰ��ϵ�д�
�����Ŀ
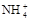 )�����ǣ� ��
)�����ǣ� ��