题目内容
【题目】(1)乙醇(C2H5OH)是未来内燃机的首选环保型液体燃料,它可以由绿色植物的秸秆制取,1.0g乙醇完全燃烧生成液态水放出1.367kJ热量,表示乙醇燃烧热的热化学方程式_____________。
(2)断开1molAB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B键的键能。下表列出了一些化学键的键能E:
化学键 | H-H | O=O | O-H |
E/kJ·mol-1 | 436 | x | 463 |
请回答下列问题:
①如图表示某反应的能量变化关系,则此反应为________(填“吸热”或“放热”)反应,其中ΔH=__________(用含有a、b的关系式表示)。
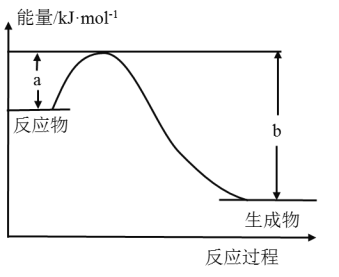
②若图示中表示反应H2(g)+![]() O2(g)=H2O(g)ΔH=-241.8kJ·mol-1,则b=_______kJ·mol-1,x=________。
O2(g)=H2O(g)ΔH=-241.8kJ·mol-1,则b=_______kJ·mol-1,x=________。
【答案】C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH=-62.882kJ·mol-1 放热 (a-b)kJ·mol-1 926 496.4
【解析】
(1)依据燃烧热的定义解答,表示燃烧热的热化学方程式中可燃物为1mol,产物为稳定氧化物;依据1g乙醇完全燃烧生成CO2和液态水时放热1.367kJ,结合燃烧热的定义计算求出1mol乙醇完全燃烧放出的热量,然后写出热化学方程式;
(2)①由图可知反应物的总能量大于生成物的总能量,属于放热反应,焓变等于断开反应物中化学键吸收的能量减去形成生成物中化学键释放的能量;
②b为1mol水中含有的化学键的键能,即为2倍的O-H的键能,根据焓变△H=反应物的键能总和-生成物的键能总和可计算出x数值。
(1)燃烧热是指:在25℃、101KPa时,1mol纯净物完全燃烧生成稳定的氧化物放出的热量;1g乙醇完全燃烧生成CO2和液态水时放热1.367kJ,则1mol乙醇,质量为46g,完全燃烧生成稳定的氧化物放出的热量为:46×1.367kJ=62.882kJ,其燃烧热的热化学方程式为:C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=62.882kJmol1;
(2)①由图可知反应物的总能量大于生成物的总能量,属于放热反应,焓变等于断开反应物中化学键吸收的能量减去形成生成物中化学键释放的能量,因此△H=(ab)kJmol1;
②b为1mol水中含有的化学键的键能,即为2倍的OH的键能,因此b=2×463kJmol1=926kJmol1,根据焓变△H=反应物的键能总和生成物的键能总和可得:436+![]() 463×2=241.8,求得x=496.4。
463×2=241.8,求得x=496.4。

 名校课堂系列答案
名校课堂系列答案