题目内容
【题目】(1)已知甲、乙两物质分别由H、C、Na、O、Cl、Fe元素中的一种或几种组成,请按要求填空:
①若甲物质为碱性氧化物,则甲的化学式为___________________(写一种)。
②若乙物质可用于呼吸面具中作为氧气来源,则乙是___________,其供氧原理是__________(用化学方程式表示)。
(2)在横线上填入合适的符号:________+2H+=CO2↑+H2O+Ba2+
(3)写出氯气与水反应的化学方程式,并用双线桥法标出电于转移的方向和数目:______________________________________________________。
(4)选择合适的试剂除去下列括号内的杂质。(填化学式)
物质 | 选择的试剂 |
①FeCl2(FeCl3) | ______ |
②NO气体(NO2) | _____________ |
【答案】 Na2O或Fe2O3 Na2O2(过氧化钠) 2Na2O2+2CO2=2Na2CO3+O2 BaCO3 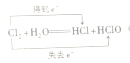 Fe H2O
Fe H2O
【解析】(1)①碱性氧化物与酸反应生成盐和水,所以甲物质可以为氧化钠或氧化铁;甲的化学式为Na2O或Fe2O3;正确答案:Na2O或Fe2O3。
②若乙物质可用于呼吸面具中作为氧气来源,则乙是过氧化钠,其供氧原理是2Na2O2+2CO2=2Na2CO3+O2;正确答案:Na2O2(过氧化钠);2Na2O2+2CO2=2Na2CO3+O2。
(2)通过原子守恒、电荷守恒规律可知,碳酸钡固体与盐酸反应生成二氧化碳,所以横线上物质为BaCO3,正确答案:BaCO3。
(3)氯气与水反应生成盐酸和次氯酸,1mol氯气完全反应,转移电子数为NA,具体如下:
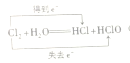 ;正确答案:
;正确答案:
(4)FeCl3溶液中加入足量的铁粉,再过滤,可以得到纯净的FeCl2;NO2能够与水反应生成NO气体和硝酸,通过洗气即可达到目的,正确答案:Fe ; H2O。

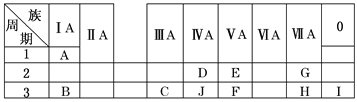
【题目】X~W是元素周期表中的短周期元素,其性质或结构信息如下表:
元素 | X | Y | Z | V | W |
性质信息 | 单质为有色气体,有毒,可用于自来水消毒 | 日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着 | 其单质在空气中约占4/5左右 | 单质为淡黄色晶体,质脆,不溶于水,微溶于酒精 | 位于第ⅣA,是形成的化合物最多的元素之一 |
回答下列问题:
(1)X在元素周期表中的位置是____________,V2-离子结构示意图为______________。
(2)Z的单质特别稳定,原因在于_______________;X、Y和V三元素中原子半径最小的是_________。
(3)WV2常温下呈液态,是一种常见的溶剂。已知WV2在氧气中完全燃烧,生成VO2和WO2,若0.1 mol WV2在1 mol O2中完全燃烧,则所得气体混合物在标准状况下的体积为________L。