题目内容
【题目】[化学——选修3:物质结构与性质]
元素A、B、C、D、E、F、G在元素周期表中的位置如下图所示,回答下列问题:

(1)G的基态原子核外电子排布式为________。原子的第一电离能:D________E(填“>”或“<”)。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l-l > l-b > b-b(l为孤对电子对,b为键合电子对),则关于A2C中的A-C-A键角可得出的结论是________。
A.180° B.接近120°,但小于120°
C.接近120°,但大于120° D.接近109°28’,但小于109°28’
(3)化合物G(BC)5的熔点为-20℃,沸点为103℃,其固体属于________晶体,该物质中存在的化学键类型有________,它在空气中燃烧生成红棕色氧化物,反应的化学方程式为________。
(4)化合物BCF2的立体构型为________,其中B原子的杂化轨道类型是________,写出两个与BCF2具有相同空间构型的含氧酸根离子________。
(5)化合物EC的晶胞结构如图所示,晶胞参数a=0.424nm。每个晶胞中含有___________个E2+,列式计算EC晶体的密度(g·cm-3)______________。

【答案】(1)1s22s22p63s23p63d64s2 <
(2)D
(3)分子 配位键、共价键 4Fe(CO)5+13O2![]() 2Fe2O3+20CO2
2Fe2O3+20CO2
(4)平面三角形 sp2 CO32-、NO3-
(5)4 ![]()
【解析】
试题分析:(1)根据元素周期表G是26号铁元素,Fe基态原子核外电子排布式为1s22s22p63s23p63d64s2。同周期元素第一电离能逐渐增大,原子的第一电离能:D<E。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l-l > l-b > b-b(l为孤对电子对,b为键合电子对),A是H元素、C是O元素,则H2O中的A-C-A键角可得出的结论是接近109°28’,但小于109°28’。
(3)化合物Fe(CO)5的熔点为-20℃,沸点为103℃,熔沸点较低,其固体属于分子晶体,该物质中存在的化学键类型有配位键、共价键,它在空气中燃烧生成红棕色氧化物氧化铁,反应的化学方程式为4Fe(CO)5 + 13O2 ![]() 2Fe2O3 + 20CO2。
2Fe2O3 + 20CO2。
(4)COCl2分子的结构式为 ,中心C原子形成2个单键和1个双键,共3个价层电子对,所以为sp2杂化,化合物COCl2的立体构型为平面三角形,与COCl2具有相同空间构型的含氧酸根离子CO32-、NO3-。
,中心C原子形成2个单键和1个双键,共3个价层电子对,所以为sp2杂化,化合物COCl2的立体构型为平面三角形,与COCl2具有相同空间构型的含氧酸根离子CO32-、NO3-。
(5)化合物为MgO,每个晶胞中含有4个E2+;设有1mol晶胞,则MgO的物质的量是4mol,质量是4×40g·mol-1;1mol晶胞的体积是(0.424×10-7cm)3×6.02×1023mol-1;,列式计算EC晶体的密度![]() 。
。

【题目】只给出下列甲和乙中对应的物理量,不能求出物质的量的是( )
A | B | C | D | |
甲 | 物质中的粒子数 | 标准状况下的气体摩尔体积 | 固体的体积 | 溶液中溶质的物质的量浓度 |
乙 | 阿伏加德罗常数 | 标准状况下的气体的体积 | 固体的密度 | 溶液体积 |
【题目】某研究性小组探究乙酸乙酯的反应机理,实验如下:
CH3COOH + C2H5OH ![]() CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
投料 1 : 1 CH3COOH转化率 65%
1 : 10 CH3COOH转化率 97%
(在120 ℃下测定)
已知:相关物理性质(常温常压)
密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 | |
乙醇 | 0.79 | -114 | 78 | 溶 |
乙酸 | 1.049 | 16.2 | 117 | 溶 |
乙酸乙酯 | 0.902 | 84 | 76.5 | 不溶 |
合成反应:
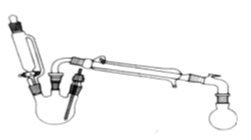
在三颈瓶中加入乙醇5 mL,硫酸5 mL,2小片碎瓷片。漏斗加入乙酸14.3 mL ,乙醇20 mL。冷凝管中通入冷却水后,开始缓慢加热,控制滴加速度等于蒸馏速度,反应温度不超过120 ℃。
分离提纯:
将反应粗产物倒入分液漏斗中,依次用少量饱和的Na2CO3溶液、饱和NaCl溶液、饱和CaCl2溶液洗涤,分离后加入无水碳酸钾,静置一段时间后弃去碳酸钾。最终通过蒸馏得到纯净的乙酸乙酯。
回答下列问题:
(1)酯化反应的机理
用乙醇羟基氧示踪
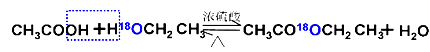
用醋酸羟基氧示踪

含氧18水占到总水量的一半,酯也一样。这个实验推翻了酯化反应为简单的取代反应。请你设想酯化反应的机理 。
2)酯化反应是一个可逆的反应,120 ℃时,平衡常数K= 。
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)浓硫酸与乙醇如何混合? 。
(5)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是? 。
(6)蒸出的粗乙酸乙酯中主要有哪些杂质? 。饱和的Na2CO3溶液洗涤除去乙酸。如何判断是否除净? 。用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水? 。