题目内容
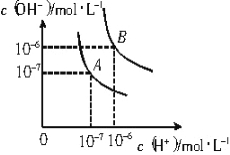
【题目】某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断正确的是

A.Ⅱ为盐酸稀释时pH的变化曲线
B.a点Kw的数值比c点Kw的数值大
C.b点溶液的导电性比c点溶液的导电性强
D.b点酸的总浓度大于a点酸的总浓度
【答案】C
【解析】
试题分析:A.醋酸是弱酸,在溶液中存在电离平衡,当稀释时,电离平衡正向移动,使溶液中c(H+)增大,溶液的pH减小,所以Ⅱ应为醋酸稀释时的pH值变化曲线,错误;B.Kw 的大小只取决于温度,所以a点Kw的数值等于c点Kw的数值,错误; C.溶液导电性取决于离子浓度,b点的H+ 浓度大,导电性强,正确;D.相同pH值的盐酸和醋酸,醋酸浓度远大于盐酸的浓度,稀释到相同体积时,醋酸(Ⅱ)浓度大于盐酸(Ⅰ)浓度,即b点酸的总浓度小于a点酸的总浓度,错误;故选C。

练习册系列答案
相关题目