题目内容
【题目】某同学想利用镁与盐酸或醋酸在不同温度下反应,探究外界条件对反应速率的影响.部分实验用表如下:
实验 | 温度/K | 盐酸浓度 | 醋酸浓度/molL﹣1 | 实验目的 |
① | 298 | 0.20 | a.实验①和②,探究温度对反应速率的影响; | |
② | 308 | 0.20 | ||
③ | 298 | 0.40 | ||
④ | 0.20 | |||
⑤ | 0.20 |
(1)请完成上工作表(填写实验④⑤的空格).
(2)上表实验①中,镁条消失的时间为20s.实验过程中,镁条剩余质量与时间关系如图: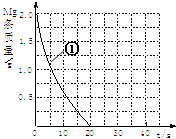
Ⅰ假设反应过程中盐酸体积不变,则要计算该反应的速率v(HCl),尚缺少的数据是 .
(3)Ⅱ若反应温度每升高10℃,反应速率增大到原来的2倍;温度相同时,醋酸是相同浓度盐酸平均速度的1/2,请在图中大致画出“实验②”、“实验④中醋酸实验”的镁条质量与时间关系曲线,并用②或④注明曲线代表的实验(假设实验中所用镁完全相同,且镁均能完全溶解).
【答案】
(1)解:根据实验目的“实验④⑤,探究温度对镁与盐酸反应和镁与醋酸反应速率的影响”,则实验④和⑤的温度不相同即可,两个实验的浓度必须相等,则实验⑤和实验④的浓度相同,故答案为:④298或308;⑤308或298,0.20,0.20;
(2)盐酸的体积
(3)解:该反应温度每升高10℃,反应速率是原来的2倍,温度相同、浓度相同时,醋酸的平均反应速度是盐酸的 ![]() ,与①比较,②温度升高10℃,反应速率是原来的2倍,所以②反应时间缩短到10min,④的反应速率是①的
,与①比较,②温度升高10℃,反应速率是原来的2倍,所以②反应时间缩短到10min,④的反应速率是①的 ![]() ,则反应时间是①的2倍,即40min,所以其图象为
,则反应时间是①的2倍,即40min,所以其图象为 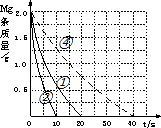 ,
,
【解析】解:Ⅱ.能够计算出消耗的HCl的物质的量,但缺少盐酸的体积,无法计算出氯化氢的浓度变化,则无法求算出盐酸的反应速率,所以答案是:盐酸的体积;