题目内容
【题目】设NA为阿伏加德罗常数的数值,则下列说法正确的是( )
A. 0.1mol·L-1的NaHSO4溶液中含有阳离子的物质的量为0.2mol
B. 在标准状态下,11.2 L NO与11.2 L O2混合后气体分子数为0.75NA
C. 含1molFeCl3的饱和溶液滴入沸水中得到氢氧化铁胶体粒子数目为NA
D. 106 g Na2CO3固体中的阴离子数为NA
【答案】D
【解析】没有溶液体积不能计算溶质的物质的量,故A错误;由于存在反应![]() ,所以在标准状态下,11.2 L NO与11.2 L O2混合后气体分子数小于0.75NA,故B错误;氢氧化铁胶粒是氢氧化铁的聚合体,所以含1molFeCl3的饱和溶液滴入沸水中得到氢氧化铁胶体粒子数目小于NA,故C错误;Na2CO3固体中的阴离子是CO32-,106 g Na2CO3固体中的阴离子数为
,所以在标准状态下,11.2 L NO与11.2 L O2混合后气体分子数小于0.75NA,故B错误;氢氧化铁胶粒是氢氧化铁的聚合体,所以含1molFeCl3的饱和溶液滴入沸水中得到氢氧化铁胶体粒子数目小于NA,故C错误;Na2CO3固体中的阴离子是CO32-,106 g Na2CO3固体中的阴离子数为![]() ,故D正确。
,故D正确。

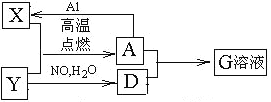
【题目】无水硫酸铜是一种重要的化学试剂,工业上用低品位钢矿(合CuS、Cu2S、CuO,以及FeO、Fe2O3、SiO2等杂质)制备无水硫酸铜的流程如下图所示:

(NH4)2SO4、CuSO4的溶解度(g)部分数据如下表所示:
温度 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
S(CuSO4)/g | 17 | 20.7 | 24.4 | 28.5 | 33.6 | 40 | 77 |
S[(NH4)SO4]/g | 73 | 75.4 | 78.1 | 81.0 | 84.5 | 87.8 | 102 |
(1)氧化与浸取过程中发生的反应之一为Cu2S被MnO2氧化时有一种非全属单质生成,则该反应的离子方程式为____________,滤渣1的主要成分是__________(填化学式),除铁时加入CuO能得到滤渣2的原理是__________________。
(2)除铁后,为了判断滤液中是否有Fe3+残留,请设计实验方案:__________。
(3)沉锰时还有一种酸性气体生成,则沉锰时发生反应的离子方程式为___________。(已知pH=8.8时,Mn2+开始沉淀)。
(4)为了从料液1中尽可能多地析出粗胆矾,操作a的内容是__________(填名称)。
(5)工业上利用上述原理制备胆矾。已知:298K时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=8.0×10-38。离子浓度小于1×10-5mol/L时表明该离子已完全沉淀。常温下,若某溶液中c(Cu2+)=2.2 mol/L,c(Fe3+)=O.001mol/L,加入氧化铜除铁时,调节溶液pH范围为________(lg5=0.7)。
【题目】现有前四周期的5种元素的部分信息如下表所示:
元素代号 | 元素部分信息 |
X | X的阴离子核外电于云均呈球形 |
Y | 原子的能级上有3个未成对电子,其最简单气态氢化物在水中的溶解度在同族元素所形成的最简单气态氢化物中最大 |
Z | 基态原于核外有3个能级填充了电子,能量最高能级的电子数等于前两个能级的电子数之和 |
R | 元素原于的围电子排布式为nsn-1npn-1 |
T | 一种核素的质量数为65,中子数为36 |
根据上述元素信息,回答下列问题:
(1)基态T2+的电子排布式为____________。
(2)Y.Z.R 的电负性由大到小的顺序为____________ (用元素符号表示)。
(3)YX4+的空间构型为____________,离子中Y原子的杂化轨道类型为____________ ,YX4+电子式为________。
(4)YX3的一种等电子体分子是______,YX3 的键角大于X2Z的键角的主要原因是________。
(5)T单质不溶于YX3溶液,也不溶于X2Z溶液,但能溶于它们的混合溶液,其主要原因是形成了稳定的[T(YX3)4]2+,1mol该阳离子中共含有______mol σ键。
(6)Z、T组成的晶胞结构如下图所示。已知Z、T原子的半径分别为apm、bpm,晶胞边长为cpm,则该晶胞中原子的空间利用率为________(用代数式表示)。