题目内容
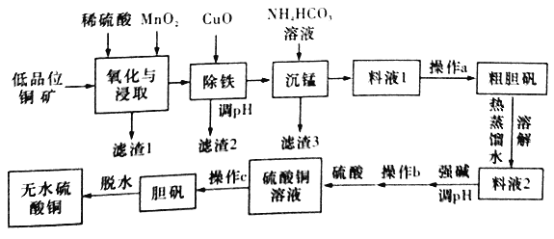
【题目】无水硫酸铜是一种重要的化学试剂,工业上用低品位钢矿(合CuS、Cu2S、CuO,以及FeO、Fe2O3、SiO2等杂质)制备无水硫酸铜的流程如下图所示:
(NH4)2SO4、CuSO4的溶解度(g)部分数据如下表所示:
温度 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
S(CuSO4)/g | 17 | 20.7 | 24.4 | 28.5 | 33.6 | 40 | 77 |
S[(NH4)SO4]/g | 73 | 75.4 | 78.1 | 81.0 | 84.5 | 87.8 | 102 |
(1)氧化与浸取过程中发生的反应之一为Cu2S被MnO2氧化时有一种非全属单质生成,则该反应的离子方程式为____________,滤渣1的主要成分是__________(填化学式),除铁时加入CuO能得到滤渣2的原理是__________________。
(2)除铁后,为了判断滤液中是否有Fe3+残留,请设计实验方案:__________。
(3)沉锰时还有一种酸性气体生成,则沉锰时发生反应的离子方程式为___________。(已知pH=8.8时,Mn2+开始沉淀)。
(4)为了从料液1中尽可能多地析出粗胆矾,操作a的内容是__________(填名称)。
(5)工业上利用上述原理制备胆矾。已知:298K时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=8.0×10-38。离子浓度小于1×10-5mol/L时表明该离子已完全沉淀。常温下,若某溶液中c(Cu2+)=2.2 mol/L,c(Fe3+)=O.001mol/L,加入氧化铜除铁时,调节溶液pH范围为________(lg5=0.7)。
【答案】 Cu2S+2MnO2+8H+=2Mn2++S+2Cu2++4H2O SiO2、S(或SiO2、S、MnO2) CuO消耗溶液中的H+,有利于Fe3+的水解平衡向右移动 从滤液中取样,滴加KSCN溶液,显血红色说明残留Fe3+,不显血红色说明无Fe3+残留(其他合理答案均可 Mn2++2HCO3-=MnCO3↓+CO2↑+H2O 蒸发浓缩、冷却结晶、过滤(洗涤) 3.3<pH≤4
【解析】本题主要考查对于工业上用低品位钢矿制备无水硫酸铜流程的评价。
(1)生成的非全属单质为S,则该反应的离子方程式为Cu2S+2MnO2+8H+=2Mn2++S+2Cu2++4H2O,滤渣1的主要成分是SiO2、S(或SiO2、S、MnO2),除铁时加入CuO能得到滤渣2的原理是CuO消耗溶液中的H+,有利于Fe3+的水解平衡向右移动。
(2)除铁后,为了判断滤液中是否有Fe3+残留,可用实验方案:从滤液中取样,滴加KSCN溶液,显血红色说明残留Fe3+,不显血红色说明无Fe3+残留(其他合理答案均可)。
(3)沉锰时还有一种酸性气体生成,该气体为二氧化碳,则沉锰时发生反应的离子方程式为Mn2++2HCO3-=MnCO3↓+CO2↑+H2O。
(4)为了从料液1中尽可能多地析出粗胆矾,操作a的内容是蒸发浓缩、冷却结晶、过滤(洗涤)。
(5)Cu2+开始沉淀时c(OH-)= 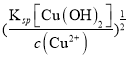 =1×10-10mol/L,pH=4,加入氧化铜除铁时,c(Fe3+)<1×10-5mol/L,c(OH-)>(
=1×10-10mol/L,pH=4,加入氧化铜除铁时,c(Fe3+)<1×10-5mol/L,c(OH-)>( 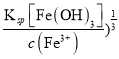 =(
=(![]() =2×10-11mol/L,c(H+)<
=2×10-11mol/L,c(H+)<  =
=![]() mol/L =5×10-4mol/L,pH>3.3,调节溶液pH范围为3.3<pH≤4。
mol/L =5×10-4mol/L,pH>3.3,调节溶液pH范围为3.3<pH≤4。

【题目】下表是元素周期表的一部分,根据所给的10 种元素,回答下列间题.
族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | C | N | F | Na | ||||
3 | Na | Mg | Al | Si | S | Cl |
(1)非金属性最强的元素是;
(2)Ne 原子结构示意图为;
(3)C 与N 中,原子半径较小的是;
(4)氯水具有漂白作用,是由于其中含有(填“HCl”或“HClO”)
(5)元素最高价氧化物对应的水化物中,碱性最强的是(填化学式),呈两性的是(填化学式);
(6)元素硅的氧化物常用于制造(填一种高性能的现代通讯材料的名称);
(7)如图为某有机物的球棍模型(其中 ![]() 代表氢原子代表
代表氢原子代表 ![]() 碳原子),
碳原子), 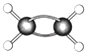 该有机物中碳元素与氢元素的质量比m(C):m(H)= . (相对原子质量C﹣12、H﹣1)
该有机物中碳元素与氢元素的质量比m(C):m(H)= . (相对原子质量C﹣12、H﹣1)
(8)镁是制造汽车、飞机、火箭的重要材料.写出工业上电解熔融氯化镁获得金属镁的化学方程式 .
【题目】(Ⅰ)工业上通常采用CO(g)和H2(g)催化合成甲醇CH3OH(g)。
(1)已知在某温度和压强下:
①2CO(g)+O2(g)=2CO2(g) △H= -566.0 kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) △H= - 483.6 kJ·mol-1
③2CH3 OH(g)+3O2(g)=2CO2(g)+4H2 O(g) △H= -1275.6 kJ·mol-1
则在相同的温度和压强下,CO(g)与H2(g)合成CH3OH(g)的热化学方程式是_________________________________________________________。
(2)某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为2L的密闭容器内充入1 molCO和 2 molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,甲醇的物质的量的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
甲醇/mol | 0 | 0.22 | 0.36 | 0.45 | 0.5 | 0.5 |
则从反应开始到20min时,以CO表示的平均反应速率=_________________,该温度下平衡
常数K=________________,若升高温度则K值__________(填“增大”、“减小”或“不变”);
(3)下列描述中能说明上述反应已达平衡的是________________;
A.2 v (H2)正= v (CH3OH)逆 B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变 D.单位时间内生成 n molCO 的同时生成 2n molH2
(Ⅱ)回答下列问题:
(1)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则Ka(HX) ______ Ka(CH3COOH)(填>、<或=)
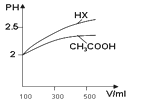
(2)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中C(CH3COO)- c(Na+)=________mol·L-1(填精确值)。