题目内容
【题目】周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。
回答下列问题:
(1)b、c、d中第一电离能最大的是____________(填元素符号),e的价层电子排布图为_________。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为_________;分子中既含有极性共价键、又含有非极性共价键的化合物是__________(填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是_________(任写一种);酸根呈三角锥结构的酸是___________(填化学式)。
(4)e和c形成的一种离子化合物的晶体结构如图1所示,则e离子的电荷为__________。
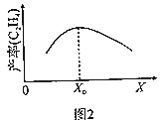
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中,阴离子为__________,阳离子中存在的化学键类型有____________;该化合物加热时首先失去的组分是____________,判断理由是___________________。

【答案】N  sp3 H2O2、N2H4 HNO2(或HNO3) H2SO3 +1 SO42- 共价键、配位键 H2O H2O与Cu2+之间的配位键比NH3与Cu2+的弱
sp3 H2O2、N2H4 HNO2(或HNO3) H2SO3 +1 SO42- 共价键、配位键 H2O H2O与Cu2+之间的配位键比NH3与Cu2+的弱
【解析】
周期表前四周期的元素a、b、c、d、e,原子序数依次增大,a的核外电子总数与其周期数相同,则a为H元素;c的最外层电子数为其内层电子数的3倍,最外层电子数不超过8个,则c是O元素;b的价电子层中的未成对电子有3个,且原子序数小于c,则b是N元素;e的最外层只有1个电子,但次外层有18个电子,则e原子核外电子数为2+8+18+1=29,为Cu元素;d与c同族,且原子序数小于e,所以d为S元素,据此解答。
(1)同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第ⅡA族和第VA族元素第一电离能大于其相邻元素,同一主族元素中,元素第一电离能随着原子序数增大而减小,所以b、c、d元素第一电离能最大的是N元素;e的价层电子为3d、4s电子,其价层电子排布图为 ;
;
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子为NH3,该分子的中心原子含有3个共价单键和一个孤电子对,所以N原子的杂化方式为sp3;分子中既含有极性共价键、又含有非极性共价键的化合物有H2O2和N2H4;
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是HNO2、HNO3;酸根呈三角锥结构的酸是H2SO3;
(4)该晶胞中c离子个数=1+8×![]() =2,e离子个数4,该晶胞中氧离子和铜离子个数之比=2:4=1:2,所以e和c形成的一种离子化合物化学式为Cu2O,则e离子的电荷为+1;
=2,e离子个数4,该晶胞中氧离子和铜离子个数之比=2:4=1:2,所以e和c形成的一种离子化合物化学式为Cu2O,则e离子的电荷为+1;
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,说明该阴离子价层电子对个数是4且不含孤电子对,为SO42-;阳离子呈轴向狭长的八面体结构,根据图知,其阳离子中铜离子配位数是8,在八面体上下顶点上分子含有两个共价键且含有两个孤电子对,为水分子,有两个,正方形平面上四个顶点上分子含有3个共价键且含有一个孤电子对,所以为氨气分子,有4个,所以阳离子中含有配位键和共价键;H2O和Cu2+的配位键比NH3与Cu2+的弱,所以该化合物加热时首先失去的组分是H2O。

 阅读快车系列答案
阅读快车系列答案【题目】CuAlO2是重要化工品,(NH4)2Fe(SO4)2·6H2O(摩尔盐)是化学上常用的分析试剂。某小组以黄铜矿(主要成分是CuFeS2,含少量SiO2)为原料制备这两种化工品,流程如图:
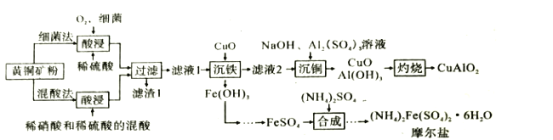
已知:①几种氢氧化物的开始沉淀和完全沉淀的pH,如表所示。
Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀/pH | 4.7 | 7.6 | 2.7 |
完全沉淀/pH | 6.7 | 9.6 | 3.7 |
②4CuO+4Al(OH)3![]() 4CuAlO2+6H2O+O2↑
4CuAlO2+6H2O+O2↑
回答下列问题:
(1)CuAlO2中铜的化合价为__;滤渣1的主要成分是__(填化学式)。
(2)反应物中铁元素被氧化的目的是__。
(3)提高这两种方案中“酸浸”反应速率都需要加热,但温度都不宜过高,其原因是__。
(4)在混酸法中,CuFeS2溶于混酸生成Cu2+,Fe3+,SO42-和一种无色气体,该气体遇空气迅速变为红棕色。写出CuFeS2与混酸反应的离子方程式__。
(5)评价上述流程,补充完整:
优点 | 缺点 | |
细菌法 | ①__ | 化学反应慢,需要时间长 |
混酸法 | 节省时间 | ②___ |