��Ŀ����
����Ŀ��ijУ��ѧ����С��Ϊ�˼���̼���ƺ�̼���������ְ�ɫ���壬�ò�ͬ�ķ�����������ʵ�飬��ͼ����ʾ��
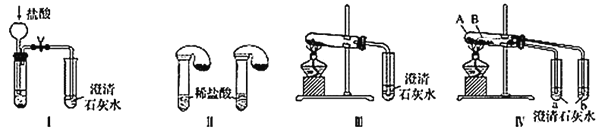
(1)ֻ����ͼ����ʾʵ�飬�ܹ��ﵽʵ��Ŀ�ĵ���________(��װ�����)��
(2)ͼ����ʾʵ����ܼ������������ʣ��䷴Ӧ�Ļ�ѧ����ʽΪ__________����ʵ�����ȣ�ʵ������ŵ���_____(����ĸ)��
A.���Ȣ���
B.���Ȣ�ȫ
C.���Ȣ�������
D.������������һ��װ��ͬʱ���������Ա�ʵ�飬������
(3)����ʵ�����֤̼���ƺ�̼�����Ƶ��ȶ��ԣ����Թ�B��װ��Ĺ��������________(�ѧʽ)��ʵ������е�����Ϊ__________��
(4)�������Ϸ����������پٳ�һ��������ߵķ�����__________��
���𰸡��� 2NaHCO3![]() Na2CO3��H2O��CO2����CO2��Ca(OH)2=CaCO3����H2O D NaHCO3 a�г���ʯ��ˮ����ǣ�b�г���ʯ��ˮ������� �Ѷ��߷ֱ������Һ��μ�BaCl2�Լ����а�ɫ�������ɵ�ΪNa2CO3���������ΪNaHCO3
Na2CO3��H2O��CO2����CO2��Ca(OH)2=CaCO3����H2O D NaHCO3 a�г���ʯ��ˮ����ǣ�b�г���ʯ��ˮ������� �Ѷ��߷ֱ������Һ��μ�BaCl2�Լ����а�ɫ�������ɵ�ΪNa2CO3���������ΪNaHCO3
��������
(1)̼���ơ�̼�����ƾ����������ᷴӦ����������̼����̼�����������ᷴӦ�����ʴ���̼���ƣ�
(2) ̼����ֱ�Ӽ��Ȳ��ֽ⣬��̼�����Ƽ�������̼���ơ�������̼���塢ˮ��
(3)̼����ֱ�Ӽ��Ȳ��������壬��̼�����Ʋ�ֱ�Ӽ��ȾͲ������壬����˵��̼�����Ʋ��ȶ���
(4)Na2CO3���Ȼ�����Ӧ����̼�ᱵ������NaHCO3���Ȼ�������Ӧ��
(1)ͼ�����ܴﵽʵ��Ŀ�ģ���Ϊ����̼���ƻ���̼�����ƾ����������ᷴӦ����������̼��������̼���������ʯ��ˮ���ñ���ǣ��ʲ����ԣ�ͼ�����Լ�����Ϊ��������̼���ƺ�̼��������������ϡ���ᷴӦ�����ɵĶ�����̼���������ͬ���ɸ����������ͳ̶����жϡ�
(2)ͼ���������漰�Ļ�ѧ����ʽΪ2NaHCO3![]() Na2CO3��H2O��CO2����CO2��Ca(OH)2=CaCO3����H2O��ʵ�������ŵ��ǿ�ͬʱ���Ա�ʵ�飬��ѡD��
Na2CO3��H2O��CO2����CO2��Ca(OH)2=CaCO3����H2O��ʵ�������ŵ��ǿ�ͬʱ���Ա�ʵ�飬��ѡD��
(3)̼����ֱ�Ӽ��Ȳ��������壬��̼�����Ʋ�ֱ�Ӽ��ȾͲ������壬����˵��̼�����Ʋ��ȶ��������Թ�B��װ��Ĺ��������̼�����ƣ��۲쵽������Ϊa�г���ʯ��ˮ����ǣ�b�г���ʯ��ˮ������ǡ�
(4)����Na2CO3��NaHCO3��������������Һ�е�����������ӵIJ�ͬ����ѡ���Լ���CO32����Ba2����Ca2����Ӧ���ɰ�ɫ������HCO3����Ba2����Ca2������Ӧ�����Կ������Ȼ�����Һ����Na2CO3��NaHCO3��

 ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д� �ݾ�ѵ������ϵ�д�
�ݾ�ѵ������ϵ�д� С����ȫ�ܼ��ϵ�д�
С����ȫ�ܼ��ϵ�д�����Ŀ��ij�о���ѧϰС������H2C2O4��Һ������KMnO4��Һ�ķ�Ӧ̽������������ĸı�Ի�ѧ��Ӧ���ʵ�Ӱ����������������ʵ�飺
ʵ����� | ʵ�� �¶�/K | �й����� | ��Һ��ɫ������ɫ����ʱ��/s | ||||
����KMnO4��Һ | H2C2O4��Һ | H2O | |||||
V/mL | c/mol��L-1 | V/mL | c/mol��L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
��1��ͨ��ʵ��A��B����̽����___(���ⲿ����)�ĸı�Ի�ѧ��Ӧ���ʵ�Ӱ�죬����V1��____��T1��____��ͨ��ʵ��___(��ʵ�����)��̽�����¶ȱ仯�Ի�ѧ��Ӧ���ʵ�Ӱ�죬����V2��____��
��2����t1��8�����ɴ�ʵ����Եó��Ľ�����_____��������Һ����ı仯������ʵ��B�����ݼ��㣬0��8s�ڣ���KMnO4��Ũ�ȱ仯��ʾ�ķ�Ӧ����v(KMnO4)��___��
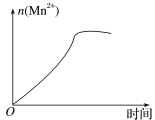
��3����С���һλͬѧͨ���������Ϸ��֣�����ʵ�������n(Mn2+)��ʱ��ı仯�����ͼ��ʾ������Ϊ������ֱ仯��ԭ���Ƿ�Ӧ��ϵ�е�ij�����Ӷ�KMnO4�����֮��ķ�Ӧ��ij���������ã����������____����Ӧ�������������___(�����ӷ���)��
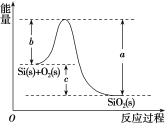
����Ŀ����֪����1mol������к���2molSi��Si����
��Si(s)��O2(g)===SiO2(g) ��H���䷴Ӧ�����������仯��ͼ��ʾ��
��
��ѧ�� | Si��O | O=O | Si��Si |
�Ͽ�1 mol���ۼ���������/kJ | 460 | 500 | 176 |
����˵������ȷ���ǣ� ��
A.������������ǽ���ѧ��ת��Ϊ����B.���������ȶ���С�ڹ���ȶ���
C.��H����988kJ��mol��1D.��H��(a��c)kJ��mol��1
����Ŀ���±����г���25 �桢101 kPaʱһЩ���ʵ�ȼ��������:
���� | CH4(g) | CH3OCH3(g) | H2(g) | HC��CH(g) |
ȼ����/(kJ��mol-1) | 890.3 | 1 453.0 | 285.8 | 1 299.6 |
��֪:��1 molҺ̬ˮ��Ϊ��̬ˮҪ����44.0 kJ��������
�ڼ���:C��H����413.4 kJ��mol-1��H��H����436.0 kJ��mol-1��
���������������
A. CH3OCH3(g)+3O2(g)��2CO2(g)+3H2O(l)����H=-1 453.0 kJ��mol-1
B. C��C���ļ���Ϊ786.0 kJ��mol-1
C. 2CH4(g)+O2(g)��CH3OCH3(g)+H2O(g)����H=-283.6 kJ��mol-1
D. H2O(g)��H2O(l)����H=-44.0 kJ��mol-1