题目内容
微量元素硒(Se)对人体有保健作用,已知硒为第四周期第ⅥA族元素,根据它在周期表中的位置推测,下列对硒元素性质的描述不正确的是( )
| A、硒化氢不稳定 |
| B、最高氧化物的化学式是SeO3 |
| C、硒与铁反应可生成FeSe |
| D、酸性强弱顺序:H2SeO4>H2SO4 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A.同主族自上而下非金属性减弱,非金属性越强氢化物越稳定,结合硫化氢稳定性分析;
B.最高正化合价等于族序数,书写最高价氧化物化学式;
C.Se非金属性比S弱,与Fe反应得到亚铁化合物;
D.非金属性越强,最高价含氧酸的酸性越强.
B.最高正化合价等于族序数,书写最高价氧化物化学式;
C.Se非金属性比S弱,与Fe反应得到亚铁化合物;
D.非金属性越强,最高价含氧酸的酸性越强.
解答:
解:A.硒与S同主族,非金属性S>Se,稳定性H2S>H2Se,而硫化氢不稳定,故则硒的氢化物H2Se不稳定,故A正确;
B.Se位于元素周期表中的第四周期第ⅥA族,最高化合价为+6价,最高价氧化物为SeO3,故B正确;
C.因Se非金属性比S弱,则硒与Fe反应生成低价化合物FeSe,故C正确;
D.非金属性S>Se,最高价氧化物的水化物的酸性H2SO4>H2SeO4,故D错误;
故选D.
B.Se位于元素周期表中的第四周期第ⅥA族,最高化合价为+6价,最高价氧化物为SeO3,故B正确;
C.因Se非金属性比S弱,则硒与Fe反应生成低价化合物FeSe,故C正确;
D.非金属性S>Se,最高价氧化物的水化物的酸性H2SO4>H2SeO4,故D错误;
故选D.
点评:本题考查元素周期律,比较基础,注意根据同主族元素性质的相似性和递变性解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述中合理的是( )
| A、白酒中含有的塑化剂成分主要为邻苯二甲酸酯类,其官能团是苯基和羧基 |
| B、测定Cu(NO3)2?nH2O中结晶水的含量可用方法:称量样品→加热→冷却→恒重操作后→得到脱去结晶水后的Cu(NO3)2质量 |
| C、SO2和FeSO4溶液都能使KMn04溶液紫色褪去,但原理不同 |
| D、敞开体系中,向FeSO4溶液中滴加NaOH溶液的离子反应方程式是:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓ |
已知:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol.向1L 0.5mol/L的NaOH溶液中加入下列物质:①稀盐酸;②浓H2SO4;③稀醋酸,恰好完全反应的热效应△H1、△H2、△H3的关系正确的是( )
| A、△H1>△H2>△H3 |
| B、△H3>△H1>△H2 |
| C、△H1=△H3>△H2 |
| D、△H2>△H1>△H3 |
以下有关氨及铵盐的叙述中,不正确的是( )
| A、可以用浓氨水加热制取氨气 |
| B、铵态氮肥不能与碱性物质如草木灰混合施用 |
| C、氨的喷泉实验体现了氨的溶解性和氧化性 |
| D、氨具有还原性,一定条件下可与氧化性的物质如氧气发生反应 |
已知有机物A与NaOH的醇溶液混合加热得产物C和溶液D.C与乙烯混合在催化剂作用下可反应生成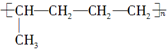 的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
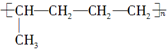 的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )A、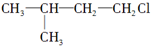 |
B、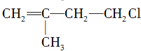 |
| C、CH3-CH2-CH2Cl |
D、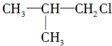 |
将金属钠分别投入下列物质的水溶液中,产生气体和蓝色沉淀的是( )
| A、NaCl |
| B、K2SO4 |
| C、CuCl2 |
| D、MgCl2 |
研究表明:多种海产品如虾、蟹、牡蛎等,体内含有+5价的砷(As)元素,但它对人体是无毒的,砒霜的成分是As2O3,属剧毒物质,专家忠告:吃饭时不要同时大量食用海鲜和青菜,否则容易中毒,并给出了一个公式:大量海鲜+大量维生素C=砒霜.下面有关解释不正确的应该是( )
| A、青菜中含有维生素C |
| B、维生素C具有还原性 |
| C、致人中毒过程中砷发生还原反应 |
| D、砒霜是氧化产物 |
下列物质中,水解的最终产物含有葡萄糖的是( )
| A、油脂 | B、蛋白质 | C、蔗糖 | D、酶 |