��Ŀ����
����Ŀ��ij��ѧ��ȤС������й�±�ؼ��仯������Ʊ�������̽��ʵ�飬��ͬѧ�Dz������ǵ�ʵ�鲢�ش��������⡣
��ʵ��һ���������Ʊ�������
(1)����ͼ��ʾ��ʵ��װ�����Ʊ���������������������������������ķ�Ӧ��ÿ�����߿��ʾһ����Ԫװ�ã������д������_____������ĸ��ţ���
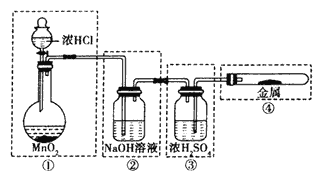
A.ֻ�Тں͢� B.ֻ�Т� C.ֻ�Тٺ͢� D.�ڢۢ�
��ʵ�����±�ػ����������ʵ��̽��
��֪�Ȼ��������۵�674�桢�е�1023�棻���Ȼ�����100������ʱ������������ˮ������ǿ�ҵ���ˮ�ԡ���500���������Ȼ��������������ܷ������ַ�Ӧ���磺12FeCl2+3O2![]() 2Fe2O3+8FeCl3��4FeCl2+3O2
2Fe2O3+8FeCl3��4FeCl2+3O2![]() 2Fe2O3+4Cl2�ȡ�����ȤС��ѡ�����²���װ�ã��г�װ��ʡ�ԣ�װ�ò����ظ�ѡ�ã������Ȼ�������������Ӧ�����̽����
2Fe2O3+4Cl2�ȡ�����ȤС��ѡ�����²���װ�ã��г�װ��ʡ�ԣ�װ�ò����ظ�ѡ�ã������Ȼ�������������Ӧ�����̽����
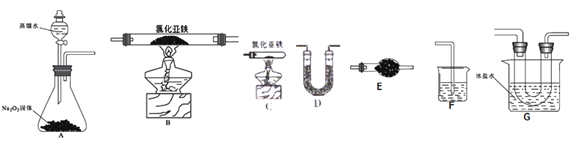
(2)ʵ��װ�õĺ�������˳��Ϊ��A��____________��F��
(3)Aװ���з�Ӧ�Ļ�ѧ����ʽΪ________________��
(4)������װ���г�ַ�Ӧ�����µĹ�����_________������ʵ��װ�õ���Ҫȱ����_____________��
(5)���÷�Ӧ���ɵ�FeCl3���ʵ��֤��Fe(OH)3�����ʵ�鷽��Ϊ____________��
��ʵ������±�ػ����ﷴӦʵ����������̽��
(6)�ڲ�ͬʵ��������KClO3�ɽ�KI����ΪI2��KIO3����С�������һϵ��ʵ�����о���Ӧ�����Է�Ӧ���Ӱ�죬����ijһʵ������ݼ�¼����(ʵ������������½���)��
�Թܱ�� | 1 | 2 | 3 | 4 |
0.20mol��L-1KI��Һ/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0mol/L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
����ˮ/mL | 9.0 | 6.0 | 3.0 | 0 |
ʵ������ |
�ٸ���ʵ���Ŀ����________________________��
�����1���Թ�ʵ���������_______________________��
����2���Թ�ʵ������Ϊ����Ӧ����Һ�ʻ�ɫ����ȡ��������Һ���������Һ����ɫ��������������Ψһ����ԭ����ΪKCl����˷�Ӧ�����ӷ���ʽΪ__________________��
���𰸡� D D(E)��B��G��E(D) 2Na2O2+2H2O=4NaOH+O2�� Fe3O4�������� B�ij������ܺ�G�Ľ����������ױ��Ȼ���������� ȡ�����Ȼ��������ˮ�ܽ⣬��pH��ֽ����pH�ƣ������Һ�����ԡ� �о���Ӧ���ֵ����ȶԷ�Ӧ�����Ӱ�죨̽�������Ũ�ȶԷ�Ӧ��Ӱ���̽����Һ���Ե�ǿ���Է�Ӧ��Ӱ�죩 ��������ʵ�� ClO3-+6I-+6H+=Cl-+3I2+3H2O
��������(1)�Ʊ���Cl2Ҫ���ñ���ʳ��ˮ��ȥHCl���壬��ͨ��Ũ��������ͨ������������Լ��õ�NaOH��Һ�������е�����Ӧ�����̳������ܲ����ܷ��ѡD��(2)A�Ʊ�O2��BFeCl2��O2��Ӧ��C�ܷ⣬��������D�����ȥˮ������E�����ֹ�ⲿ�����е�ˮ�������뷴Ӧװ�ã�F�����ڳ�ȥβ������ʵ��װ�õĺ�������˳��Ϊ��A�� D(E)��B��G��E(D)��F��(3)Aװ���з�Ӧ�Ļ�ѧ����ʽΪ2Na2O2+2H2O=4NaOH+O2����(4)��Ӧ���ɵ�����Ũ�ȸߣ�������Ϣ��500���������Ȼ��������������ܷ������ַ�Ӧ��������װ���г�ַ�Ӧ�����µĹ�����Fe3O4�������������Ȼ�����100������ʱ��������ȴ�����γɹ��壬����ʵ��װ�õ���Ҫȱ����B�ij������ܺ�G�Ľ����������ױ��Ȼ������������(5)���÷�Ӧ���ɵ�FeCl3���ʵ��֤��Fe(OH)3�������������FeCl3��ǿ�������Σ�ˮ��֮������ԣ��������Ϊ��ȡ�����Ȼ��������ˮ�ܽ⣬��pH��ֽ����pH�ƣ������Һ�����ԡ�(6)�ٴӱ������ݿ��Կ�����0.20mol��L-1KI��Һ���������ͬ��KClO3(s)��������ͬ��H2SO4��Һ������ˮ�����ڱ仯����H2SO4��Һ������ˮ���������ͬ�����Ը���ʵ���Ŀ�����о���Ӧ���ֵ����ȶԷ�Ӧ�����Ӱ�죨̽�������Ũ�ȶԷ�Ӧ��Ӱ���̽����Һ���Ե�ǿ���Է�Ӧ��Ӱ�죩��1���Թ���û�м��ᣬ���1���Թ�ʵ�����������������ʵ�飻�ۼ��������Һ����ɫ��˵��I�D���������˷�Ӧ�����ӷ���ʽΪ ClO3-+6I-+6H+=Cl-+3I2+3H2O��

 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д� ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
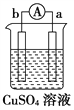
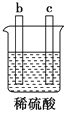
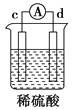
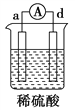
ͬ����չ�Ķ�ϵ�д�����Ŀ����a��b��c��d�ĸ������缫���йص�ʵ��װ�ü�����ʵ���������£�
ʵ�� װ�� |
װ��һ |
װ�ö� |
װ���� |
װ���� |
����ʵ������ | a��������С��b���������� | b�������������c���ޱ仯 | d���ܽ⣬c����������� | ������a�� ����d�� |
�ɴ˿��ж������ֽ������˳����( ����)
A. a��b��c��d B. b��c��d��a C. a��b��d��c D. d��a��b��c