题目内容
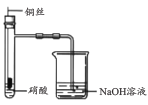
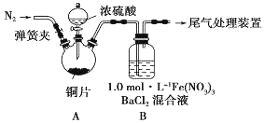
【题目】原电池原理的发现和各种电池的发明,改变了人们的生活方式。下图所示原电池装置的相关说法中,不正确的是
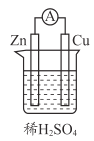
A.能将化学能转化为电能
B.电子从 Cu 经导线流向 Zn
C.溶液中H+、![]() 分别向铜、锌电极移动
分别向铜、锌电极移动
D.该装置中发生的总反应为: Zn + 2H+ = Zn2+ + H2↑
【答案】B
【解析】
A.原电池就是一种将化学能直接转化为电能的装置,故该装置能将化学能转化为电能,A正确;
B.原电池中电子是由负极经导线流向正极,该电池中Zn是负极,Cu是正极,故电子从 Zn经导线流向Cu,B错误;
C.原电池内部电流方向与外电路电流方向相反,故电解质溶液中阳离子流向正极,阴离子流向负极,故溶液中H+、![]() 分别向铜、锌电极移动,C正确;
分别向铜、锌电极移动,C正确;
D.该装置中负极发生:Zn -2e- = Zn2+,正极发生:2H+ +2e-=H2↑,故总反应为: Zn + 2H+ = Zn2+ + H2↑,D正确;
故答案为:B。

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
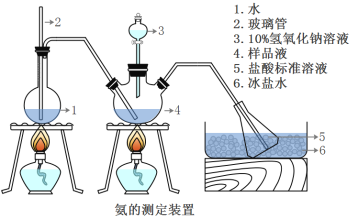
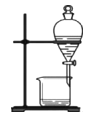
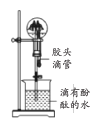
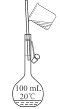
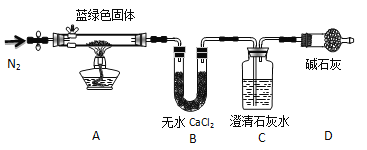
【题目】下列实验装置或操作与实验目的不相符的是
|
|
|
|
A. 证明铜与硝酸的反应 | B. 分离乙醇和乙酸的混合液 | C. 证明氨气易溶于水且水溶液呈碱性 | D. 配制100 mL0.100 mol/LNaCl溶液 |
A.AB.BC.CD.D