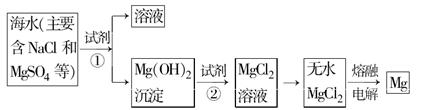
题目内容
Ⅰ.工业上用铝土矿制取铝的流程如下:
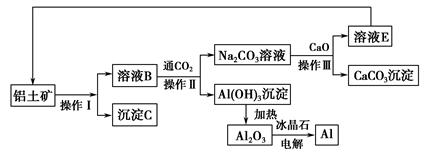
请回答下列问题:
(1)操作Ⅰ、操作Ⅱ、操作Ⅲ都用到的玻璃仪器有__________________________。
(2)写出由溶液B生成Al(OH)3的离子方程式:____________________________。
(3)工艺流程中涉及氧化还原反应的化学方程式为:_________________________。
(4)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有________(填化学式)。用此法制取铝的副产品是________(填化学式)。
Ⅱ.我国高炉生产各方面取得了显著进步,但在资源和能源利用率、高炉大型化、提高产业集中度以及环保等方面还跟国际存在很大差距,有待进一步提高,努力向钢铁强国迈进。请回答下列问题:
(1)高炉炼铁的原料有铁矿、焦炭和石灰石,其中起熔剂作用的是________,目的是除去铁矿石中的脉石,其产物密度比铁________,所以在铁水的________(填“上部”或“下部”)形成炉渣而与铁水分离。
(2)焦炭在高炉炼铁中起着举足轻重的作用,下列不属于焦炭作用的是________。
A.作为燃料,为炼铁中的化学反应提供能量
B.作为还原剂与二氧化碳反应产生还原氧化铁的一氧化碳
C.对高炉中的物料起到支撑和疏散的作用
D.作为溶剂,除去铁矿石中的杂质
(3)高炉炼铁的污染非常严重,目前我国部分大城市中的钢铁厂借着搬迁的机会也在进行着工艺改进。高炉炼铁导致的环境污染有________。
A.臭氧空洞 B.酸雨 C.一氧化碳毒害 D.沙尘暴
(4)写出高炉炼铁中与碳元素有关的氧化还原反应化学方程式:____________________________。
(5)从“三废”利用、环境保护等角度考虑,钢铁企业在生产中应采取的一些措施有(举出2种措施即可) _______________________________________。

请回答下列问题:
(1)操作Ⅰ、操作Ⅱ、操作Ⅲ都用到的玻璃仪器有__________________________。
(2)写出由溶液B生成Al(OH)3的离子方程式:____________________________。
(3)工艺流程中涉及氧化还原反应的化学方程式为:_________________________。
(4)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有________(填化学式)。用此法制取铝的副产品是________(填化学式)。
Ⅱ.我国高炉生产各方面取得了显著进步,但在资源和能源利用率、高炉大型化、提高产业集中度以及环保等方面还跟国际存在很大差距,有待进一步提高,努力向钢铁强国迈进。请回答下列问题:
(1)高炉炼铁的原料有铁矿、焦炭和石灰石,其中起熔剂作用的是________,目的是除去铁矿石中的脉石,其产物密度比铁________,所以在铁水的________(填“上部”或“下部”)形成炉渣而与铁水分离。
(2)焦炭在高炉炼铁中起着举足轻重的作用,下列不属于焦炭作用的是________。
A.作为燃料,为炼铁中的化学反应提供能量
B.作为还原剂与二氧化碳反应产生还原氧化铁的一氧化碳
C.对高炉中的物料起到支撑和疏散的作用
D.作为溶剂,除去铁矿石中的杂质
(3)高炉炼铁的污染非常严重,目前我国部分大城市中的钢铁厂借着搬迁的机会也在进行着工艺改进。高炉炼铁导致的环境污染有________。
A.臭氧空洞 B.酸雨 C.一氧化碳毒害 D.沙尘暴
(4)写出高炉炼铁中与碳元素有关的氧化还原反应化学方程式:____________________________。
(5)从“三废”利用、环境保护等角度考虑,钢铁企业在生产中应采取的一些措施有(举出2种措施即可) _______________________________________。
Ⅰ.(1)烧杯、漏斗、玻璃棒
(2)2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32—
(3)2Al2O3(熔融) 4Al+3O2↑
4Al+3O2↑
(4)CaO和CO2 Fe2O3和O2
Ⅱ.(1)石灰石 小 上部 (2)D (3)BC
(4)C+O2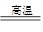 CO2;CO2+C
CO2;CO2+C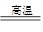 2CO;Fe2O3+3CO
2CO;Fe2O3+3CO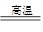 2Fe+3CO2
2Fe+3CO2
(5)用炼铁厂的炉渣(或CaSiO3)作为水泥厂的原料;用发电厂的煤矸石和粉煤灰作为水泥厂的原料;将石灰石煅烧成生石灰,用于吸收发电厂和焦化厂燃煤时产生的SO2,减少对空气的污染;建立污水处理系统(任选两条,其他合理答案也可以)
(2)2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32—
(3)2Al2O3(熔融)
 4Al+3O2↑
4Al+3O2↑(4)CaO和CO2 Fe2O3和O2
Ⅱ.(1)石灰石 小 上部 (2)D (3)BC
(4)C+O2
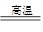 CO2;CO2+C
CO2;CO2+C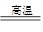 2CO;Fe2O3+3CO
2CO;Fe2O3+3CO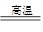 2Fe+3CO2
2Fe+3CO2(5)用炼铁厂的炉渣(或CaSiO3)作为水泥厂的原料;用发电厂的煤矸石和粉煤灰作为水泥厂的原料;将石灰石煅烧成生石灰,用于吸收发电厂和焦化厂燃煤时产生的SO2,减少对空气的污染;建立污水处理系统(任选两条,其他合理答案也可以)
Ⅰ.(1)操作Ⅰ、操作Ⅱ、操作Ⅲ都是过滤,过滤需要烧杯、漏斗、玻璃棒。(2)NaAlO2溶液中通入CO2生成Al(OH)3沉淀和Na2CO3,其离子方程式为2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32—。(3)只有电解熔融Al2O3的反应属于氧化还原反应。(4)得到的CaCO3受热分解得到CaO、CO2,可见CaO、CO2可循环使用。操作Ⅰ所得的Fe2O3和电解熔融Al2O3得到的O2为副产品。
Ⅱ.(1)高炉炼铁的原料中必须有合适比例的石灰石,其作用是作为杂质的溶剂,目的就是除去铁矿石中的二氧化硅,使其转化为熔点比较低的硅酸钙,反应为CaCO3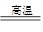 CaO+CO2↑,CaO+SiO2
CaO+CO2↑,CaO+SiO2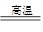 CaSiO3。硅酸钙的密度比熔融铁的密度低,所以在高炉中硅酸钙等炉渣是浮在铁水之上的。
CaSiO3。硅酸钙的密度比熔融铁的密度低,所以在高炉中硅酸钙等炉渣是浮在铁水之上的。
(2)焦炭在高炉炼铁中的作用是提供能量(作为燃料)、作为还原剂、还有对其中的物料起到支撑和疏散的作用。
(3)高炉炼铁产生的尾气中含有大量的CO、CO2、粉尘和硫、氮的氧化物,所以高炉炼铁会加剧酸雨的发生,还会导致局部地区中的CO浓度过大,使周围生物受到毒害。
(4)高炉炼铁中,根据焦炭的作用,可以写出其燃烧反应、与二氧化碳的反应、一氧化碳还原氧化铁的反应。
(5)从“三废”利用、环境保护等角度考虑,钢铁企业在生产中应建立污水处理系统;将石灰石煅烧成生石灰用于吸收发电厂和焦化厂燃煤时产生的SO2,减少对空气的污染;用发电厂的煤矸石和粉煤灰作为生产水泥的原料;用炼铁厂的炉渣作为生产水泥的原料。
Ⅱ.(1)高炉炼铁的原料中必须有合适比例的石灰石,其作用是作为杂质的溶剂,目的就是除去铁矿石中的二氧化硅,使其转化为熔点比较低的硅酸钙,反应为CaCO3
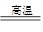 CaO+CO2↑,CaO+SiO2
CaO+CO2↑,CaO+SiO2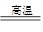 CaSiO3。硅酸钙的密度比熔融铁的密度低,所以在高炉中硅酸钙等炉渣是浮在铁水之上的。
CaSiO3。硅酸钙的密度比熔融铁的密度低,所以在高炉中硅酸钙等炉渣是浮在铁水之上的。(2)焦炭在高炉炼铁中的作用是提供能量(作为燃料)、作为还原剂、还有对其中的物料起到支撑和疏散的作用。
(3)高炉炼铁产生的尾气中含有大量的CO、CO2、粉尘和硫、氮的氧化物,所以高炉炼铁会加剧酸雨的发生,还会导致局部地区中的CO浓度过大,使周围生物受到毒害。
(4)高炉炼铁中,根据焦炭的作用,可以写出其燃烧反应、与二氧化碳的反应、一氧化碳还原氧化铁的反应。
(5)从“三废”利用、环境保护等角度考虑,钢铁企业在生产中应建立污水处理系统;将石灰石煅烧成生石灰用于吸收发电厂和焦化厂燃煤时产生的SO2,减少对空气的污染;用发电厂的煤矸石和粉煤灰作为生产水泥的原料;用炼铁厂的炉渣作为生产水泥的原料。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目