题目内容
5.随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现.下列有关说法中,正确的是( )| A. | N5+离子中含有36个电子 | B. | O2与O4属于同位素 | ||
| C. | C60是有机物 | D. | H2与H3属于同种元素组成的单质 |
分析 A.根据阳离子中核外电子数=核内质子数-离子所带电荷数;
B.根据质子数相同,中子数不同的原子互称同位素;
C.有机物的特点是:是化合物,含有碳元素,C60是一个分子中含有60个碳原子的单质;
D.H2与H3属于由同种元素形成的不同单质.
解答 解:A.因N5+中的电子数为7×5-1=34,故A错误;
B.因质子数相同,中子数不同的原子互称同位素,而O2与O4是由氧元素形成的不同单质,两者是同素异形体,故B错误;
C.C60的一个分子中含有60个碳原子,有机物必须是含有碳元素的化合物,故C错误;
D.H2与H3属于由同种氢元素形成的不同单质,故D正确;
故选D.
点评 本题考查了电子数的计算、同位素、有机物的辨析等问题,把握概念是解题的关键,题目较简单.

练习册系列答案
相关题目
15.重水(D2O)是重要的核工业原料,下列说法错误的是( )
| A. | 1H218O与D216O的相对分子质量相同 | |
| B. | H2O与D2O互称同素异形体 | |
| C. | 氘(D)原子核外有1个电子 | |
| D. | 1H与D互为同位素 |
20.下列说法中正确的是( )
| A. | 1 mol Al3+含有的核外电子数为3×6.02×1023 | |
| B. | 将58.5 g NaCl溶于1.00 L水中,所得NaCl溶液的浓度为1.00 mol•L-1 | |
| C. | 2 mol SO2气体与足量的O2在一定条件下反应,转移的电子数为4×6.02×1023 | |
| D. | 常温下,100mL pH=1的硫酸溶液中含有的H+离子数为0.01×6.02×1023 |
15.下列除去杂质的操作中,能达到目的是( )
| A. | 除去苯中的少量溴:加入CCl4萃取后分液 | |
| B. | 除去乙烷中的乙烯:通入酸性高锰酸钾溶液中 | |
| C. | 除去CO2中的少量HCl气体:通过盛有饱和Na2CO3溶液的洗气瓶 | |
| D. | 除去FeCl2溶液中的少量FeCl3:加入足量Fe粉后过滤 |
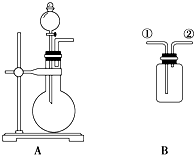 如图A是实验室制取某些气体的装置.
如图A是实验室制取某些气体的装置. 一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.
一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.

 HCO3-+OH-,与油污发生反应,达到去污目的.
HCO3-+OH-,与油污发生反应,达到去污目的.