题目内容
下列各组离子在指定溶液中一定能大量共存的是( )
| A.能使甲基橙呈红色的溶液:Ba2+、A13+、NO3-、C1- |
| B.由水电离出的c(H+)=1×10-11mol·L-1的溶液:Na+、Mg2+、Cl-、NO3- |
| C.0.2 mol·L-1的NaNO3溶液:H+、Fe2+、SO42-、Cl- |
| D.与Fe反应生成H2的溶液:NH4+、K+、SO42-、CO32- |
A
解析试题分析:A、使甲基橙呈红色的溶液显酸性,离子均能共存,正确;B、由水电离出c(H+)=1×10-11 mol·L-1,溶液可能呈酸性也可能呈碱性,Mg2+在碱性条件下不能共存,错误;C、NO3-、H+和Fe2+在溶液中发生氧化还原反应,错误;D、酸性溶液与Fe反应生成H2,溶液中H+与CO32-不能共存,错误。
考点:考查离子反应以及离子共存,涉及氢离子浓度的计算,元素化合物知识等。

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
下列离子方程式书写正确的是
| A.铁溶于稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| B.二氧化硫与足量烧碱溶液反应:S02+20H-=S032-+H20 |
| C.醋酸溶液与氢氧化钠溶液反应:H++OH-=H20 |
D.浓盐酸与MnO2反应制Cl2:Mn02+2H++2C1- C12↑+Mn2++H20 C12↑+Mn2++H20 |
下列叙述不正确的是
| A.易溶于水的物质一定是电解质 |
| B.有化学键断裂的变化不一定是化学变化 |
| C.溶解于水所得溶液能导电的物质不一定是电解质 |
| D.水受热不易分解,与水分子之间存在的氢键无关 |
下列物质的水溶液能导电,但属于非电解质的是
| A.NH3 | B.Cl2 | C.C2H5OH | D.CH3COOH |
下列各组离子在制定的溶液中一定能大量共存的是
| A.无色溶液:K+、Al3+、NO3-、AlO2- |
| B.pH=12的溶液:K+、Cl-、SO32- 、SiO32- |
| C.含0.1mol?L-1 NO3-的溶液:H+、Fe3+、Cl-、SO42- |
| D.由水电离产生的c(H+)=1×10-12 mol?L—1的溶液:Na+、NH4+、SO42-、HCO3- |
向15mL 0.1mol/L Ba(OH)2溶液中,滴加等浓度NH4Al(SO4)2溶液x mL,下列叙述错误的是
| A.x=5时,溶液中有Ba2+、OH-、AlO2-,且OH-> AlO2- |
| B.x=7.5时,溶液中有NH4+、AlO2-,且NH4+=AlO2- |
| C.x=10时,溶液中有SO42-、NH4+,且H+> OH- |
| D.x=15时,溶液中有SO42-、NH4+、Al3+,且NH4+> Al3+ |
下列离子方程式正确的是
| A.大理石溶于醋酸: CaCO3+2H+ =Ca2+ + CO2 ↑ +H2O |
| B.FeBr2溶液中通入少量的Cl2: Cl2+2Fe2+=2Fe3+ +2Cl- |
| C.向NaHSO4溶液中滴加Ba(OH)2至刚好沉淀完全:2H++SO42- +Ba2+ +2OH- = BaSO4 ↓+ ↑2H2O |
| D.酸性氢氧燃料电池的正极反应: H2-2e- = 2H+ |
下列离子方程式正确的是
| A.向AlCl3溶液中滴加氨水:Al3++3OH-=Al(OH)3↓ |
| B.向NaHCO3溶液中加入少量Ca(OH)2溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O |
C.向苯酚溶液中滴加Na2CO3溶液: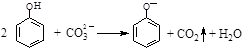 |
| D.向氯化亚铁溶液中滴加稀硝酸:3Fe2++4H++ NO3-= 3Fe3++NO↑+2H2O |
25℃时,下列各组离子在指定溶液中能大量共存的是
| A.滴人甲基橙显红色的溶液中:NH4+、Ba2+、AlO—2、CI— |
B.Kw/c( H+) =0.l mol/L的溶液:Na+、K+、Si 、HC 、HC |
C.含有较多S '的溶液:H+、Ca2+、Fe3+、N '的溶液:H+、Ca2+、Fe3+、N |
D.澄清透明溶液中:K+、M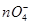 、H3O+、SO42― 、H3O+、SO42― |