题目内容
4.下列醇既能发生消去反应,又能被氧化为醛的是( )| A. | CH3OH | B. |  | C. |  | D. |  |
分析 醇能发生消去反应,说明连接醇羟基的碳原子相邻碳原子上含有氢原子,醇能被氧化生成醛,说明醇羟基位于边上,据此分析解答.
解答 解:醇能发生消去反应,说明连接醇羟基的碳原子相邻碳原子上含有氢原子,醇能被氧化生成醛,说明醇羟基位于边上,
A.甲醇中只有一个碳原子,不能发生消去反应,故A错误;
B.2-丙醇被氧化生成酮而不是醛,故B错误;
C.该分子中连接醇羟基的碳原子相邻碳原子上没有氢原子,不能发生消去反应,故C错误;
D.该分子中醇羟基位于边上且连接醇羟基碳原子相邻碳原子上含有氢原子,所以能发生消去反应、能被氧化生成醛,故D正确;
故选D.
点评 本题考查有机物结构和性质,明确官能团及其性质关系即可解答,注意醇发生消去反应时醇分子结构特点,为易错点.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
14.已知钋的原子序数是84,是一种放射性元素,被称为世界上最毒的物质,是推测它在周期表的位置( )
| A. | 第四周期第ⅢA族 | B. | 第六周期第ⅥA族 | C. | 第五周期第ⅥA族 | D. | 第六周期第ⅦA族. |
12.X、Y、M、N是短周期主族元素,且原子序数依次增大.已知X的最外层电子数是电子层数的3倍,X、M同主族,Y原子在短周期主族元素中原子半径最大.下列说法正确的是( )
| A. | M与X形成的化合物对应的水化物一定是强酸 | |
| B. | Y2X和Y2X2中阴、阳离子的个数比相同,化学键类型也完全相同 | |
| C. | X、Y的简单离子半径:r(X2-)>r(Y+) | |
| D. | X的气态氢化物比M的气态氢化物稳定 |
19.已知某元素原子的各级电离能数值如下:I1=736kJ/mol,I2=1450kJ/mol,I3=7740kJ/mol,I4=10500kJ/mol,则该元素的化合价为( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
9.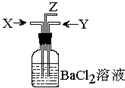 碳跟浓硫酸共热产生的气体X和二氧化锰跟浓盐酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是…( )
碳跟浓硫酸共热产生的气体X和二氧化锰跟浓盐酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是…( )
 碳跟浓硫酸共热产生的气体X和二氧化锰跟浓盐酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是…( )
碳跟浓硫酸共热产生的气体X和二氧化锰跟浓盐酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是…( )| A. | 洗气瓶中产生的沉淀是碳酸钡 | |
| B. | 在Z导管出来的气体中无二氧化碳 | |
| C. | 洗气瓶中产生的沉淀是硫酸钡 | |
| D. | 洗气瓶中产生的沉淀是碳酸钡和亚硫酸钡 |
16.下列几组化合物,化学键类型不相同的是( )
| A. | NH3和H2O | B. | Na2O和MgCl2 | C. | H2S和Na2S | D. | NaOH和NH4Cl |
13.下列对于硝酸的认识,不正确的是( )
| A. | 浓硝酸和稀硝酸都具有氧化性 | |
| B. | 铜与浓硝酸的反应是置换反应 | |
| C. | 常温下,可用铁或铝制容器盛放浓HNO3 | |
| D. | 往少量的浓硝酸中加入足量的铜,生成的气体只有NO2 |
14.某无色透明的酸性溶液能与铁反应生成氢气,则该溶液中一定能够大量共存的是( )
| A. | NH4+、K+、Ba2+、Cl- | B. | Na+、K+、Cl-、SiO32- | ||
| C. | SO42-、Na+、Cu2+、Cl- | D. | SO42-、NO3-、K+、Na+ |

 .
. ;⑤n CH2=CHCH2COOH$\stackrel{催化剂}{→}$
;⑤n CH2=CHCH2COOH$\stackrel{催化剂}{→}$ .
. .
.