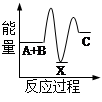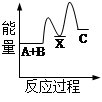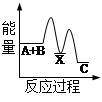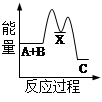题目内容
下列关于化学反应的描述中正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.已知NaOH(aq) +HCI(aq) =NaCI(aq)+H2O(1) △H= 一57.3 kJ·mol-1, 则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出57.3 kJ的热量 |
| C.CO(g)的燃烧热是283.0 kJ·mol-1,则表示CO(g)的燃烧热的热化学方程式为 2CO (g)+ O2(g)=2CO2(g) △H=一283.0 kJ·mol-1 |
| D.已知2C(s) +2O2(g)=2CO2(g) △H=a, 2C(s) +O2(g)="2CO" (g) △H=b,则b>a |
D
解析试题分析:A、吸热和放热反应由反应物和生成物总能量的相对高低决定,与是否需要加热无关,错误;B、醋酸为弱酸,电离过程吸热,故放出的热量小于57.3kJ,错误;C、燃烧热为1mol物质完全燃烧生成稳定物质时候放出的热量,错误;D、两个反应均为放热反应,△H小于零,放热量越多,代数值越小。正确。
考点:热化学相关的概念。

练习册系列答案
相关题目
肼(H2N—NH2)是一种高能燃料,有关化学反应的能量变化,如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则断裂1molN—H键所需的能量(kJ)是
| A.194 | B.391 |
| C.516 | D.658 |
已知25℃、10lkPa条件下: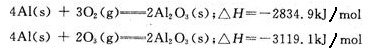
由此得出的正确结论是
| A.等质量的O2比O3能量低,由O2变O3为吸热反应 |
| B.等质量的O2比O3能量低,由O2变O3为放热反应 |
| C.O3比O2稳定,由O2变O3为吸热反应 |
| D.O2比O3稳定,由O2变O3为放热反应 |
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是( ) 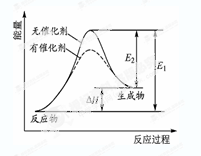
| A.该反应为放热反应 |
| B.催化剂能改变该反应的焓变 |
| C.催化剂能降低该反应的活化能 |
| D.逆反应的活化能大于正反应的活化能 |
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是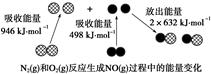
| A.1molN2(g)和NA个O2(g)反应放出的能量为180kJ |
| B.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量 |
| C.通常情况下,N2(g)和O2(g)混合能直接生成NO |
| D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
① CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0 kJ/mol
② CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9 kJ/mol
下列说法正确的是
| A.CH3OH的燃烧为吸热反应 |
B.反应①中的能量变化如图所示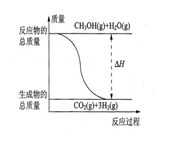 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
| D.根据②推知反应:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H >-192.9kJ/mol |
在容积固定不变的密闭容器中加入1mol N2和3mol H2发生反应:N2(g)+3H2(g) 2NH3(g) △H=" —92.4" kJ·mol-1,下列结论正确的是
2NH3(g) △H=" —92.4" kJ·mol-1,下列结论正确的是
| A.该反应达到平衡时,放出的热量等于92.4kJ |
| B.达到平衡后向容器中通入1mol氦气,平衡不移动 |
| C.降低温度和缩小容器体积均可使该反应的平衡常数增大 |
| D.若达到平衡时N2的转化率为20%,则平衡时容器内的压强是起始时的90% |