题目内容
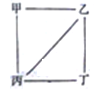
【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证哪位同学的判断正确,丙同学设计了如图所示实验装置(锌与浓硫酸共热时产生的气体为X,气体发生装置略去)。试回答:

(1)上述反应中生成二氧化硫的化学方程式为__________________。
(2)乙同学认为还可能产生氢气的理由是__________________。
(3)丙同学在安装好装置后,必须首先进行的一步操作是:_________________。
(4)A中加入的试剂可能是________,作用是__________________;
B中加入的试剂可能是________,作用是__________________;
E中加入的试剂可能是________,作用是____________________。
(5)可以证明气体X中含有氢气的实验现象是:C中:________,D中:________。如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?________(填“能”或“不能”),原因是________________________。
【答案】 Zn+2H2SO4(浓)![]() ZnSO4+SO2↑+2H2O 当Zn与浓硫酸反应时,浓硫酸浓度逐渐变小,Zn与稀硫酸反应可产生H2 检查装置的气密性 品红溶液 检验SO2 浓硫酸 吸收水蒸气 碱石灰 防止空气中的水蒸气进入D中 黑色(CuO)粉末变成红色(Cu) 白色粉末变成蓝色 不能 因为混合气体中可能含水蒸气,会干扰H2的检验
ZnSO4+SO2↑+2H2O 当Zn与浓硫酸反应时,浓硫酸浓度逐渐变小,Zn与稀硫酸反应可产生H2 检查装置的气密性 品红溶液 检验SO2 浓硫酸 吸收水蒸气 碱石灰 防止空气中的水蒸气进入D中 黑色(CuO)粉末变成红色(Cu) 白色粉末变成蓝色 不能 因为混合气体中可能含水蒸气,会干扰H2的检验
【解析】(1)锌和浓硫酸反应是二氧化硫、硫酸锌和水,反应的化学方程式为Zn+2H2SO4(浓)![]() ZnSO4+SO2↑+2H2O (浓),因此,本题正确答案是: Zn+2H2SO4(浓)
ZnSO4+SO2↑+2H2O (浓),因此,本题正确答案是: Zn+2H2SO4(浓)![]() ZnSO4+SO2↑+2H2O ;
ZnSO4+SO2↑+2H2O ;
(2)反应时浓H2SO4(浓)浓度逐渐变稀,Zn与稀H2SO4反应可产生H2,和硫酸锌,反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;因此,本题正确答案是: 当Zn与浓硫酸反应时,浓硫酸浓度逐渐变小,Zn与稀硫酸反应可产生H2。
(3)装置是气体验证食盐,所以需要装置气密性完好,实验开始先检验装置的气密性,因此,本题正确答案是:检查装置的气密性。
(4)分析装置图可以知道,生成的气体中有二氧化硫和氢气,所以装置A是验证二氧化硫存在的装置,选品红溶液进行验证;通过高锰酸钾溶液除去二氧化硫,通过装置B中的浓硫酸除去水蒸气,利用氢气和氧化铜反应生成铜和水蒸气,所以利用装置D中 的无水硫酸铜检验水的生成,为避免空气中的水蒸气影响D装置中水的检验,装置E中需要用碱石灰,因此,本题正确答案是:品红溶液; 检验SO2;浓硫酸;吸收水蒸气;碱石灰;防止空气中的水蒸气进入D中。
(5)证明生成的气体中含有氢气的现象,C装置中黑色氧化铜变为红色铜,D装置中白色硫酸铜变为蓝色,因此,本题正确答案是:黑色的CuO变成红色的Cu,白色粉末变成蓝色。去掉装置B,高锰酸钾溶液中的水蒸气可能会使D中出现蓝色,但不能根据此现象判断气体X中有氢气。答案:不能 . 因为混合气体中可能含水蒸气,会干扰H2的检验。

 名校课堂系列答案
名校课堂系列答案【题目】试回答下列各题:
(1)如图1所示是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: ______________________________。
(2)化学反应的焓变与反应物和生成物的键能有关。
①已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1

请填空:
共价键 | H—H | Cl—Cl | H—Cl |
键能/(kJ·mol-1) | 436 | 247 | ________ |
②图2中表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢在热力学标准状态下,发生分解反应的热化学方程式: ___________________________________。