题目内容
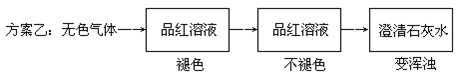
(1)设计一个简单的一次性完成实验的装置,验证醋酸、二氧化碳水溶液(碳酸)和苯酚的酸性,其强弱的顺序是:CH3COOH> H2CO3> C6H5OH
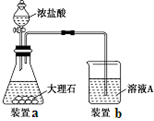
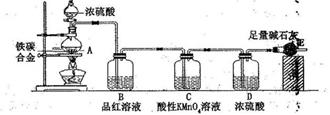
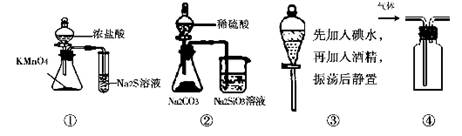
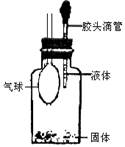
①利用下列仪器可以组装实验装置,则仪器的连接顺序是: 。
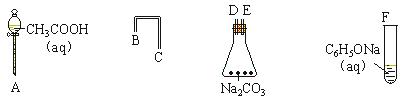
②写出实验过程中发生反应的离子方程式。 、 。
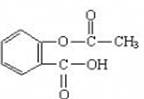
(2)若1 mol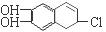 分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是 mol和 mol。
分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是 mol和 mol。
①利用下列仪器可以组装实验装置,则仪器的连接顺序是: 。
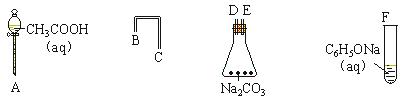
②写出实验过程中发生反应的离子方程式。 、 。
(2)若1 mol
 分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是 mol和 mol。
分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是 mol和 mol。(10分)(1)ADEBCF(2)2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑
H2O+CO2+C6H5O-→ C6H5OH+HCO3- (2)3 和 3
H2O+CO2+C6H5O-→ C6H5OH+HCO3- (2)3 和 3
试题分析:(1)根据较强的酸制备较弱的酸可知,要证明醋酸的酸性强于碳酸的,则应该将醋酸滴入碳酸钠中,然后将生成的CO2通入到苯酚钠中即可,所以正确的连接顺序是ADEBCF。
(2)实验过程中发生反应的离子方程式有2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑、H2O+CO2+C6H5O-→ C6H5OH+HCO3-。
(3)根据有机物的结构简式可知,分子中含有2个酚羟基、1个氯原子、1个碳碳双键,所以能和2mol单质溴发生取代反应,1mol溴发生加成反应,共计是3mol。2mol酚羟基需要2mol氢氧化钠,1mol氯原子水解又需要1mol氢氧化钠,共计是3mol。
点评:该题是基础性试题的考查,试题侧重对学生基础知识的巩固和训练,意在培养学生灵活运用基础知识解决实际问题的能力。该题的关键是记住常见官能团的结构、性质以及官能团之间的相互转化,然后结合题意灵活运用即可,有利于培养学生的逻辑推理能力和规范的实验设计能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目