题目内容
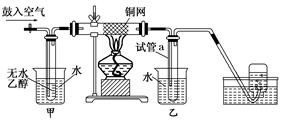
某校化学兴趣小组设计了如下实验装置(图中部分夹持仪器已略去)来测定某铁碳合金中铁的质量分数,并探究铁与浓硫酸的反应。
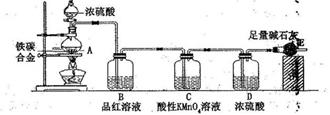
请回答下列问题:
(1)mg铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现彖,其原因是①_____②_____
(2)点燃酒精灯,可观察到B中的现象是_____________________,C 的作用是___________________
(3)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。则铁碳合金中铁的质量分数为________________(写表达式)。
(4)兴趣小组使用设计的如图实验装置,操作正确,且每一个反应均完全,仍然发现所测得的铁碳合金中铁的质量分数偏低,其主要原因是________________。
(5)若反应一段时间后,用滴管吸取A中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:
I:只含有Fe3+; II:只含有Fe2+;III:________________________
验证III的实验方法是________________________

请回答下列问题:
(1)mg铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现彖,其原因是①_____②_____
(2)点燃酒精灯,可观察到B中的现象是_____________________,C 的作用是___________________
(3)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。则铁碳合金中铁的质量分数为________________(写表达式)。
(4)兴趣小组使用设计的如图实验装置,操作正确,且每一个反应均完全,仍然发现所测得的铁碳合金中铁的质量分数偏低,其主要原因是________________。
(5)若反应一段时间后,用滴管吸取A中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:
I:只含有Fe3+; II:只含有Fe2+;III:________________________
验证III的实验方法是________________________
(1)常温下碳与浓硫酸不反应,常温下Fe遇浓硫酸发生钝化
(2)品红溶液褪色,或“颜色变浅”;除尽反应产物中的SO2气体
(3)(11m-3b)/11m
(4)干燥管中的碱石灰吸收了空气中的二氧化碳、水蒸气等
(5)既有Fe2+又有Fe3+
取试样少许于试管中,先滴加少量的KSCN溶液,振荡后溶液显红色证明有Fe3+;再取试样少许于另一支试管中,滴加少量的酸性KMnO4溶液,若浅红色褪去,证明溶液中含有Fe2+。
试题分析:(1)常温下,碳与浓硫酸不反应,Fe遇浓硫酸发生钝化,因此无明显现象。
(2)点燃酒精灯后,反应开始,碳与浓硫酸反应可生成CO2和SO2,Fe与浓硫酸反应生成SO2,B装置检验SO2,现象是品红褪色,C装置除尽SO2,D装置干燥气体,E装置吸收CO2。
(3)E增重的是CO2的质量,bgCO2中C的质量为
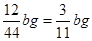 ,因此Fe的质量分数为
,因此Fe的质量分数为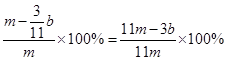 。
。(4)该实验的原理是通过测量CO2的量计算铁的质量分数,CO2的质量通过干燥管E的实验前后质量差获得,干燥管右侧直接通空气,则空气中的CO2、水蒸气都可能进入干燥管中,使CO2的质量偏大,铁的质量分数偏小。
(5)结合前两种可能,则第三种是既有Fe2+又有Fe3+。检验Fe3+一般用KSCN,现象是溶液显红色,检验Fe2+一般利用其还原性,用酸性KMnO4溶液检验,现象是浅红色褪去。

练习册系列答案
相关题目
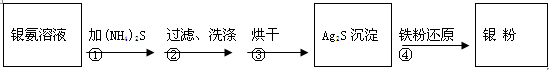
 2 Ag+ FeCl2+H2S↑。
2 Ag+ FeCl2+H2S↑。
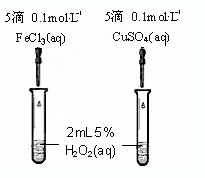
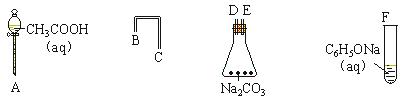
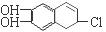 分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是 mol和 mol。
分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是 mol和 mol。