题目内容
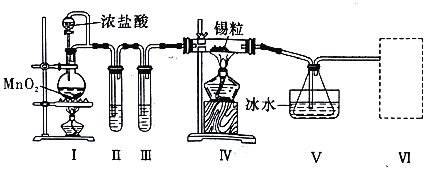
【题目】某化学小组的同学设计了如下实验装置制备SnCl4。
已知:①金属锡熔点为231℃,化学活泼性与铁相似;
②纯净而干燥的氯气与熔融金属锡反应生成SnCl4,SnCl4的沸点为114℃;
③SnCl4易与水反应。
请根据上图装置回答:
(1)裝置I中发生反应的离子方程式是______________。
(2)试管II中的试剂是________,试管III中的试剂是____________。
(3)装置V的作用是____________。
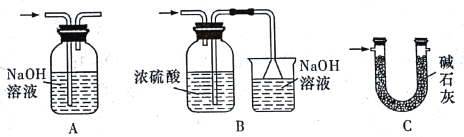
(4)裝置Ⅵ 最好选用下列装置中的____(填标号)。
(5)实验结束后,欲回收利用装置Ⅰ中未反应完的MnO2,需要的玻璃仪器有_________。
【答案】 MnO2 + 4H++ 2Cl-![]() Mn2+ +Cl2↑+2H2O 饱和食盐水 浓硫酸 冷凝(收集)SnCl4 C 漏斗、玻璃棒、烧杯
Mn2+ +Cl2↑+2H2O 饱和食盐水 浓硫酸 冷凝(收集)SnCl4 C 漏斗、玻璃棒、烧杯
【解析】根据图及实验目的知,I是制备Cl2的装置,加热条件下,浓盐酸和MnO2反应生成Cl2;浓盐酸具有挥发性,气体亦可携带水蒸气,所以得到的Cl2中含有HCl、H2O杂质;一般用饱和食盐水除去HCl,再用浓硫酸吸水,所以装置II中装有饱和食盐水吸收HCl,装置III中装有浓硫酸干燥氯气。纯净的Cl2与锡反应生成SnCl4,SnCl4的沸点为114℃,沸点较低,所以装置V冰水浴降温,冷凝得到SnCl4液体。
(1)浓盐酸和MnO2反应的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
故答案为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)根据上述分析,试管II中装有饱和食盐水,试管III装有浓硫酸。
故答案为:饱和食盐水;浓硫酸;
(3)SnCl4的沸点较低,装置V中的冰水可以使得SnCl4冷凝,得到SnCl4液体;
故答案为:冷凝(收集)SnCl4;
(4)Cl2有毒,需要进行尾气处理,故装置VI应为尾气处理装置,吸收未反应完的Cl2。SnCl4易与水反应,所以不仅要除去Cl2中的水蒸气,还要防止外界水蒸气进入,所以装置VI还要能防止水蒸气进入装置V。A选项装置,NaOH可以吸收未反应完的Cl2,但不能防止水蒸气进入装置Ⅴ;B选项装置,气体进入装置中导管应该长进短出,装置错误;C选项装置,碱石灰不仅可以吸收Cl2,也可以吸收水蒸气和二氧化碳,能避免空气中二氧化碳和水蒸气进入装置Ⅴ,故选C。
故答案为:C。
(5)回收利用装置I中未反应完的MnO2,MnO2难溶于水,可以用过滤操作回收。过滤装置选择需要的仪器为:漏斗、玻璃棒、烧杯。
故答案为:漏斗、玻璃棒、烧杯。

【题目】完成下列问题:
(1)某学习小组用0.80mol/L标准浓度的氢氧化钠溶液测定未知浓度的盐酸.
①滴定管如图所示,用(填“甲”或“乙”)滴定管盛待测定的未知浓度的盐酸溶液.
②用滴定的方法来测定盐酸的浓度,实验数据如表所示:
实验编号 | 待测盐酸溶液的体积/mL | 滴入NaOH溶液的体积/mL |
1 | 20.00 | 23.00 |
2 | 20.00 | 23.10 |
3 | 20.00 | 22.90 |
该未知盐酸的浓度为(保留两位有效数字).
(2)若用酚酞作指示剂,达到滴定终点的标志是 .
(3)造成测定结果偏高的操作可能是 .
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的读数时,滴定前仰视凹液面最低处,滴定后俯视读数.