题目内容
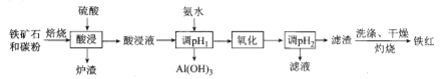
【题目】I.炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
(1)铁锅的锈蚀是________腐蚀(填“析氢”或“吸氧”)。
(2)写出铁锅腐蚀正极的电极反应式:_______________
II.在如图用石墨作电极的电解池中,放入500mL饱和NaCl溶液并滴入酚酞,进行电解,观察到B电极附近溶液先变红。请回答下列问题:

(1)A接的是电源的_______极,B是该装置______。
(2)写出电解时总反应的离子方程式:____________________________ 。
(3)电解后溶液的pH______ ;(填 增大、减小或不变)要使电解后溶液恢复到电解前的状态,则需加入_______ 。
(4)若电源为碱性锌锰干电池,负极为______ 正极为______ 电解质溶液是_______
【答案】吸氧 O2+4e-+2H2O=4OH- 正极 阴极 写出电解时总反应的离子方程式:2Cl- + 2H2O ====(电解)H2↑+Cl2↑+2OH- 增大 HCl 气体 锌 二氧化锰 氢氧化钾溶液
【解析】
I.(1)钢铁腐蚀主要是电化学腐蚀,其中又以吸氧腐蚀为主;
(2)氧气在正极得到电子,电极反应式为O2+4e-+2H2O=4OH-;
II.(1)由电解池的结构进行判断;
(2)电解饱和食盐水的离子方程式为:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-;
Cl2↑+H2↑+2OH-;
(3)电解后生成了OH-,所以溶液的pH值增大,电解过程中逸出了氢气和氯气,要使电解后溶液恢复到电解前的状态,则需加入HCl气体;
(4)碱性锌锰干电池中Zn为负极,MnO2为正极,电解质溶液是氢氧化钾溶液。
I.(1)炒过菜的铁锅因腐蚀而出现红褐色锈斑,铁锅中电解质溶液一般为弱酸性或者中性,溶解空气中一定量的氧气,发生吸氧腐蚀,故答案为:吸氧。
(2)铁锅发生吸氧腐蚀时,氧气在正极得到电子,发生还原反应,电极反应式为O2+4e-+2H2O=4OH-,故答案为:O2+4e-+2H2O=4OH-。
II.(1)根据题意“B电极附近溶液先变红”,说明B电极生成了NaOH,则B为阴极,A为阳极,与电源正极相连的是电解池的阳极,故答案为:正极,阴极。
(2)根据分析可知,氯化钠和水都被电解,所以总的反应式为2Cl-+2H2O![]() Cl2↑+H2↑+2OH-,故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-,故答案为:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-。
Cl2↑+H2↑+2OH-。
(3)电解后生成了OH-,所以溶液的pH值增大,电解过程中逸出了氢气和氯气,要使电解后溶液恢复到电解前的状态,则需加入HCl气体,故答案为:增大,HCl气体。
(4)碱性锌锰干电池总反应方程式为:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,由反应方程式可知,Zn为负极,MnO2为正极,电解质溶液是氢氧化钾溶液,故答案为:锌,二氧化锰,氢氧化钾溶液。

【题目】已知在常温下测得浓度均为0.1molL﹣1的下列四种溶液的pH如下表:
溶质 | NaHCO3 | Na2CO3 | NaF | NaClO |
pH | 8.4 | 11.6 | 7.5 | 9.7 |
(1)用离子方程式表示NaClO溶液的pH = 9.7的原因___________________________。
(2)根据盐溶液的pH,可知①Ka(HClO) ②Ka1(H2CO3) ③Ka(HF) ④Ka2(H2CO3)的由大到小顺序为_________________________________ (填序号)。
(3)将少量CO2通入NaClO溶液中,写出该反应的离子方程式:________________。
(4)常温下,将CO2通入0.1molL﹣1的Na2CO3溶液中至中性,则溶液中2c(CO32-)+ c(HCO3-)=_________________(列计算式)