题目内容
 为探究金属的腐蚀情况,某同学将锌片和铜片置于浸有饱和食盐水和酚酞的滤纸上,并构成如图所示的装置.下列判断合理的是( )
为探究金属的腐蚀情况,某同学将锌片和铜片置于浸有饱和食盐水和酚酞的滤纸上,并构成如图所示的装置.下列判断合理的是( )| A、左边铜片上有气泡冒出 |
| B、右边锌片上的反应为2Cl--2e-=Cl2↑ |
| C、最先观察到红色的区城是② |
| D、左右两边Cu片质量均不发生变化 |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:左边为原电池,Zn为负极,Cu为正极,铜上氧气得电子;右边为电解池,Cu为阴极,铜上氢离子得电子,Zn为阳极,据此分析.
解答:
解:A、左边为原电池,Zn为负极,Cu为正极,铜上氧气得电子,所以没有气泡冒出,故A错误;
B、右边为电解池,Zn为阳极,锌片上的反应为Zn-2e-=Zn2+,故B错误;
C、左边为原电池,右边为电解池,电解池中的反应速率快,所以最先观察到红色的区城是④,故C错误;
D、左右两边Cu片均不参加反应,所以Cu片质量均不发生变化,故D正确.
故选D.
B、右边为电解池,Zn为阳极,锌片上的反应为Zn-2e-=Zn2+,故B错误;
C、左边为原电池,右边为电解池,电解池中的反应速率快,所以最先观察到红色的区城是④,故C错误;
D、左右两边Cu片均不参加反应,所以Cu片质量均不发生变化,故D正确.
故选D.
点评:本题考查了原电池原理和电解池原理的应用,题目难度不大,注意把握电极的判断和电极方程式的书写.

练习册系列答案
相关题目
有关说法错误的是( )
| A、除去镁粉中的铝粉可选用烧碱 |
| B、等质量Al分别与足量浓硫酸和足量浓NaOH溶液放出等量的H2 |
| C、铝分别与足量稀盐酸和NaOH溶液反应,当两个反应放出的气体体积相同时,消耗的HCl和NaOH物质的量比为3:1 |
| D、等质量的两份铝分别和等物质的量的H2SO4与NaOH反应,若生成氢气质量比为7:8,则可推断必定是酸中的铝过量,而碱过量 |
化学反应的本质是旧化学键断裂和新化学键形成.下列关于化学反应的说法中,正确的是( )
| A、化学反应遵循能量最低原理,自发进行的化学反应都是放热反应 |
| B、化学反应遵循质量守恒定律,反应中元素种类和原子个数不变 |
| C、化学反应遵循熵增原理,自发进行的化学反应都是熵增反应 |
| D、化学反应遵循有效碰撞理论,所有的反应物分子都能进行有效碰撞 |
下列说法正确的是( )
| A、蛋白质都是结构复杂的高分子化合物,分子中都含有C、H、O、N等四种元素 |
| B、油脂在一定条件能发生水解反应,属于高分子 |
| C、棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O |
| D、“蜡烛成灰泪始干”中的“泪”主要是有机烯烃 |
常温下下列各组离子或分子在指定条件下,一定能大量共存的是( )
| A、含有较多Ca2+的无色溶液:K+、SiO32-、NO3-、Cl- |
| B、某中性溶液中:Fe3+、NH4+、SO42-、Br- |
| C、水电离出的c(H+)=10-5mol/L的溶液:K+、NH4+、Cl-、I- |
| D、加入甲基橙呈黄色的溶液:Na+、Cl2、NO3-、SO32- |
下列除杂质的方法正确的是( )
| A、用铁粉除去FeCl3溶液中少量的CuCl2 |
| B、用饱和碳酸钠溶液除去CO2中少量的SO2气体 |
| C、用过量的碱液除去H2中少量的HCl气体 |
| D、用过量的氨水除去Al3+溶液中的少量Fe3+ |
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、标准状况下,22.4L甲烷和乙炔混合气体所含的分子数为NA |
| B、12g NaHSO4晶体中含有H+离子数为0.1NA |
| C、60g乙酸分子中含共价键总数为6NA |
| D、11.2L Cl2与足量的NaOH溶液反应转移的电子数为0.5NA |
下列离子方程式中正确的是( )
| A、盐酸与碳酸钡反应:CO32-+2H+=CO2↑+H2O |
| B、碳酸钙溶于醋酸:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、硝酸银溶液中加入铜粉:Ag++Cu=Cu2++Ag |
| D、钠投入水中:2Na+2H2O=2Na++2OH-+H2↑ |
某化学兴趣小组设计以下实验方案,可从样品中提取粗产品:
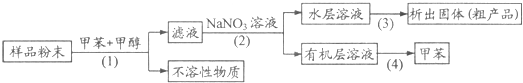
下列说法错误的是( )

下列说法错误的是( )
| A、步骤(1)需要过滤装置 |
| B、步骤(2)需要用到分液漏斗 |
| C、步骤(3)需要用到坩埚 |
| D、步骤(4)需要蒸馏装置 |