题目内容
【题目】在不同温度下,水溶液中![]() 与
与![]() 关系如图所示。下列说法不正确的是
关系如图所示。下列说法不正确的是![]()
![]()
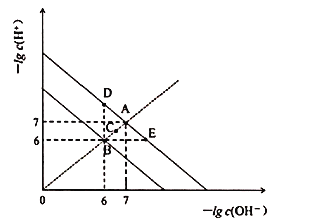
A.图中五点![]() 间的关系:
间的关系:![]()
B.![]() 点对应的水溶液中,可能有
点对应的水溶液中,可能有![]() 、
、![]() 、
、![]() 、
、![]() 大量同时存在
大量同时存在
C.若![]() 的NaHA溶液水溶液中
的NaHA溶液水溶液中![]() 与
与![]() 关系如图D点所示,则溶液中有:
关系如图D点所示,则溶液中有:![]()
D.向![]() 溶液中滴入
溶液中滴入![]() 溶液,当
溶液,当![]() 与
与![]() 关系如图E点所示,则溶液中反应:
关系如图E点所示,则溶液中反应:![]()
【答案】C
【解析】
由图象可知,A、E、D都为![]() 时的曲线上,水的Kw只与温度有关,温度相同时Kw相同,温度升高,促进水的电离,Kw增大,水的离子积只与温度有关,与溶液的类型无关,可能为纯水,也可能为酸、碱、盐溶液,据此分析解答。
时的曲线上,水的Kw只与温度有关,温度相同时Kw相同,温度升高,促进水的电离,Kw增大,水的离子积只与温度有关,与溶液的类型无关,可能为纯水,也可能为酸、碱、盐溶液,据此分析解答。
A.由图象可知,A、E、D都为![]() 时的曲线上,水的Kw只与温度有关,温度相同时Kw相同,温度升高,促进水的电离,Kw增大,则
时的曲线上,水的Kw只与温度有关,温度相同时Kw相同,温度升高,促进水的电离,Kw增大,则![]() ,由C点
,由C点![]() 可知,C点的Kw大于A点小于B,所以
可知,C点的Kw大于A点小于B,所以![]() ,故A正确;
,故A正确;
B.E点![]() ,溶液呈酸性,酸性条件下,
,溶液呈酸性,酸性条件下,![]() 、
、![]() 、
、![]() 、
、![]() 没有沉淀、气体、弱电解质、氧化还原反应产生,所以能共存,故B正确;
没有沉淀、气体、弱电解质、氧化还原反应产生,所以能共存,故B正确;
C.D点溶液中![]() ,溶液呈碱性,说明
,溶液呈碱性,说明![]() 的水解程度大于电离程度,所以
的水解程度大于电离程度,所以![]() ,故C错误;
,故C错误;
D.E点![]() ,溶液呈酸性,向
,溶液呈酸性,向![]() 溶液中滴入
溶液中滴入![]() 溶液,则溶液中反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故D正确;
溶液,则溶液中反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故D正确;
故选C。

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
【题目】某温度下,0.200 molL-1的HA溶液与0.200 molL-1的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如下表,下列说法正确的是
微粒 | X | Y | Na+ | A- |
浓度/(mol·L-1) | 8.00 | 2.50 | 0.100 | 9.92 |
A. 0.1mol·L-1HA溶液的pH=1 B. 该温度下Kw=1.0![]() 10-14
10-14
C. 微粒X表示OH-,Y表示H+ D. 混合溶液中:n(A-)+n(X)=n(Na+)