��Ŀ����
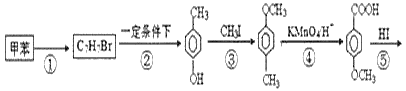
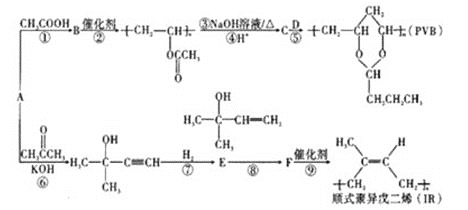
����Ŀ��A(C2H2)�ǻ����л�����ԭ�ϡ���A�Ʊ��߷��ӽ�������(PVB)��IR�ĺϳ�·��(���ַ�Ӧ������ȥ)��ͼ��ʾ��
��֪����RCHO+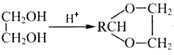 +H2O��
+H2O��
��RBr![]() RCOOH��
RCOOH��
�Իش��������⣺
��1�����̢ٵķ�Ӧ����Ϊ___��B�к��������ŵ�������___��
��2����Ӧ��Ļ�ѧ����ʽΪ___����Ӧ�۵Ļ�ѧ����ʽΪ___��
��3�����ڹ��̢ڣ�����˵����ȷ����___(�����)��
a.��Ӧ���������۷�Ӧ
b.���ɵĸ߷��ӻ����ﻹ������ˮ��Ӧ��ʹ����ɫ
c.�ø߷������ھ��к��䵥����ȫһ���Ľṹ
d.���ɵĸ߷��Ӳ��Ͼ��������ԣ���Ϊ�����
e.ͨ�������Dz�øø߷��ӵ�ƽ����Է�������Ϊ30444������֪��nԼΪ354
��4��F�����������___��ԭ�ӹ�ƽ�棬D�Ľṹ��ʽ��___��
��5��G��E��Ϊͬ���칹�壬��G������ͬ���칹���к���̼̼˫���Ľṹ(����E�����Ҳ�����˳���칹)����___�֡�(��֪̼̼˫�����ǻ�ֱ���������ȶ���������)
��6��������Ŀ��Ϣ������ϩΪ��ʼԭ�ϣ�ѡ�ñ�Ҫ�����Լ��ϳɶ������Ҷ�����д���ϳ�·��___(�ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ����)��
���𰸡��ӳɷ�Ӧ ���� 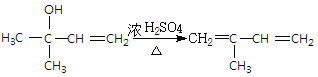 +H2O
+H2O 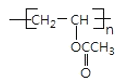 +nNaOH
+nNaOH +nCH3COONa de 11 CH3CH2CH2CHO 26
+nCH3COONa de 11 CH3CH2CH2CHO 26 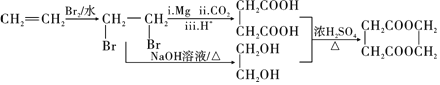
��������
�ɷ���ʽ��֪AΪCH��CH���ɸ߾���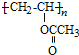 �Ľṹ����֪��Ȳ�����ᷢ���ӳɷ�Ӧ�õ�B����֪BΪCH2=CHOOCCH3����PVB�Ľṹ����֪
�Ľṹ����֪��Ȳ�����ᷢ���ӳɷ�Ӧ�õ�B����֪BΪCH2=CHOOCCH3����PVB�Ľṹ����֪![]() ����ˮ������CΪ
����ˮ������CΪ![]() ����DΪCH3CH2CH2CHO��CH��CH���ͪ��KOH�����·���̼��˫���ӳɷ�Ӧ������
����DΪCH3CH2CH2CHO��CH��CH���ͪ��KOH�����·���̼��˫���ӳɷ�Ӧ������![]() ���������������ӳɷ�Ӧ����
���������������ӳɷ�Ӧ����![]() ��F�ڴ��������µõ�˳ʽ�������ϩ
��F�ڴ��������µõ�˳ʽ�������ϩ![]()
![]()
![]() ����FΪCH2=C(CH3)CH=CH2����
����FΪCH2=C(CH3)CH=CH2����![]() ������ȥ��Ӧ����F��
������ȥ��Ӧ����F��
(1)���̢�����Ȳ�����ᷢ���ӳɷ�Ӧ����B(CH2=CHOOCCH3)��B�еĺ��������ŵ������ǣ�������
(2)��Ӧ��Ļ�ѧ����ʽΪ��![]()
![]() +H2O��
+H2O��
��Ӧ�۵Ļ�ѧ����ʽΪ��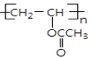 +nNaOH
+nNaOH![]()
![]() +nCH3COONa��
+nCH3COONa��
(3) a.��Ӧ�����ڼӾ۷�Ӧ��a����
b.�ø߷��Ӳ��ϲ���̼̼˫��������ˮ����Ӧ��b����
c.�ø߷�������û��̼̼˫�����䵥���к���̼̼˫�������Խṹ��ͬ��c����
d.���ɵĸ߷��Ӳ���Ϊ���ͽṹ�����������ԣ��ۺ϶Ȳ�ͬ�������ǻ���d��ȷ��
e.���ڵ���Է�������Ϊ86��ͨ�������Dz�øø߷��ӵ�ƽ����Է�������Ϊ30444������֪��n=![]() =354��e��ȷ��
=354��e��ȷ��
��ѡde��
(4)FΪCH2=C(CH3)CH=CH2������2��̼̼˫������̼̼˫��ֱ��������ԭ�Ӷ���ͬһ��ƽ���ϣ��������Ի���1��Hԭ����ͬһ��ƽ���ϣ���11���������Ϸ�����֪DΪCH3CH2CH2CHO��
(5)EΪ![]() ��G��E��Ϊͬ���칹�壬G������ͬ���칹���к���̼̼˫���Ľṹ����һ�������ſ���Ϊ�ǻ����Ѽ����纬���ǻ����ɿ���-OHȡ����ϩ��H��CH2=CH-CH2-CH2-CH3��CH3-CH=CH-CH2-CH3��CH2=C(CH3)CH2CH3��CH3C(CH3)=CHCH3��CH3CH(CH3)CH=CH2��̼̼˫�����ǻ�ֱ���������ȶ��������ǣ�-OH��ȡ����λ�ù���13�֣�
��G��E��Ϊͬ���칹�壬G������ͬ���칹���к���̼̼˫���Ľṹ����һ�������ſ���Ϊ�ǻ����Ѽ����纬���ǻ����ɿ���-OHȡ����ϩ��H��CH2=CH-CH2-CH2-CH3��CH3-CH=CH-CH2-CH3��CH2=C(CH3)CH2CH3��CH3C(CH3)=CHCH3��CH3CH(CH3)CH=CH2��̼̼˫�����ǻ�ֱ���������ȶ��������ǣ�-OH��ȡ����λ�ù���13�֣�
�纬���Ѽ�������ΪCH3-O-C4H7(8��)��CH3CH2-O-C3H5(3��)��CH3CH2CH2-O-CH=CH2��CH3C(CH3)-O-CH=CH2����13�֣����Ӧ��ͬ���칹�干26��
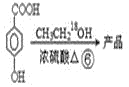
(6)���������Ҷ���������Ӧ�õ�Ŀ�����Ҫ���Ʊ����������Ҷ�������ϩ���巢���ӳɷ�Ӧ�õ�1��![]() �������飬1��
�������飬1��![]() �����������ˮ��õ��Ҷ����������Ϣ1��
�����������ˮ��õ��Ҷ����������Ϣ1��![]() ���������ڣ���Mg����CO2����H+�����µõ������ᣬ�ϳ�·������ͼΪ
���������ڣ���Mg����CO2����H+�����µõ������ᣬ�ϳ�·������ͼΪ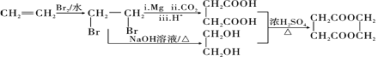 ��
��

 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
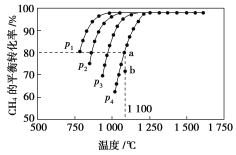
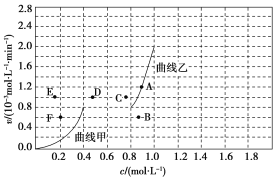
ͬ����չ�Ķ�ϵ�д�����Ŀ����ͬ�¶��£��ݻ���ͬ�ļס������������ܱ������о��������·�Ӧ��2SO2(g)+O2(g) ![]() 2SO3(g) ��H=-197 kJ/mol ��ʵ�����й��������£�
2SO3(g) ��H=-197 kJ/mol ��ʵ�����й��������£�
������� | ��ʼʱ�����ʵ����ʵ��� / mol | �ﵽƽ��ʱ��ϵ�����ı仯/kJ | ||
SO2 | O2 | SO3 | ||
�� | 2 | 1 | 0 | �ų�������Q1 |
�� | 1.8 | 0.9 | 0.2 | �ų�������Q2 |
�����ж�����ȷ����
A.�������з�Ӧ��ƽ�ⳣ�������
B.�ﵽƽ��ʱSO2�������������<��
C.197>Q1>Q2
D.����1molSO3(l)ʱ�ų�����������98.5kJ
����Ŀ���������ʣ���ͭƬ ��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() �ఱˮ��
�ఱˮ��
��1�������������ʰ����ʷ������д���±��Ŀհ״��������ʱ�ţ�
����� | ���������� | �ǵ���� | ���� |
���ڸ�������� | ___________ | ___________ | ______________ |
��2�������������ʰ����ʷ������д���±��Ŀհ״��������ʱ�ţ���
��3���ڱ�״���£���ͬ����Ģں͢ܣ���ԭ�Ӹ�����Ϊ_________��
��4��д�����������ĵ��뷽��ʽ��______________��
��5����������������������֮��ɷ������ӷ�Ӧ��![]() �������ӷ�Ӧ��Ӧ�Ļ�ѧ����ʽΪ��______________��
�������ӷ�Ӧ��Ӧ�Ļ�ѧ����ʽΪ��______________��
����Ŀ���±�ΪԪ�����ڱ���һ���֡�
̼ | �� | Y | |
X | �� | Z |
�ش���������
��1������Ԫ��ԭ�Ӱ뾶����ԭ�ӹ�ռ�ݵĹ������_________����Y���������Ų�ʽΪ________��Zԭ�Ӻ�����_____��������ͬ�ĵ��ӡ�
��2��������ʵ��˵��YԪ�صķǽ����Ա�SԪ�صķǽ�����ǿ����__________
a��Y������H2S��Һ��Ӧ����Һ�����
b����������ԭ��Ӧ�У�1molY���ʱ�1molS�õ��Ӷ�
c��Y��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
��ԭ�ӽṹ�ĽǶ�ȥ����YԪ�صķǽ����Ա�SԪ�صķǽ�����ǿ��ԭ��_______
��3��CO2�ķе�_________CS2������>������<������=������ԭ����_________________
��4�������BaCl2��Һ��ͨ������CO2���壬û�г������ɣ������μ�һ�����İ�ˮ��������ɰ�ɫ�������õ���ƽ���ƶ�ԭ��������������________
��5��������CO2ͨ��NaOH��Һ�У��õ�NaHCO3����0.1mol/L��NaHCO3��Һ�У�c(Na+)+c(H+)=________�����й�̼���Ĺ�ϵΪ��___________ = 0.1mol/L��