题目内容
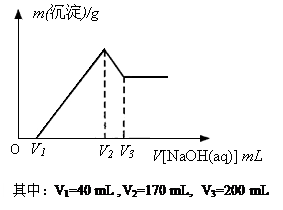
把14mL2mol/L的Al2(SO4)3溶液慢慢滴入30mL6mol/L的NaOH溶液中,并不断搅拌,随着Al2(SO4)3逐滴加入,所产生的现象是
| A.白色沉淀→沉淀增加 |
| B.白色沉淀→沉淀增加→部分溶解 |
| C.白色沉淀→沉淀随即溶解→澄清溶液 |
| D.白色沉淀→沉淀随即溶解→不再溶解→沉淀增加 |
D
向NaOH溶液中滴加Al2(SO4)3,开始因NaOH过量,生成的Al(OH)3溶解,当溶液中的NaOH完全转变为NaAlO2时,再加入Al2(SO4)3即又会出现Al(OH)3沉淀,直到NaAlO2完全转化为Al(OH)3,所以沉淀不断增加。该题简单的判断方法是:①注意滴加的是Al2(SO4)3,故开始形成的沉淀会立即消失;②根据题给两物质的量,按反应关系量简单计算是否还能出现沉淀;由1Al3+——4OH-——1AlO2-,1AlO——Al3+——2Al(OH)3,得Al3+总量=0.014×2×2="0.056" mol,OH-总量=0.03×6=0.18mol,当NaOH完全反应后,Al2(SO4)3溶液中还剩余Al3+=0.056-
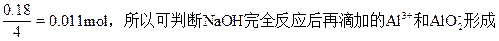
的沉淀不再溶解了。
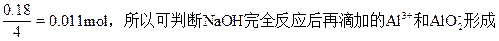
的沉淀不再溶解了。

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目