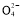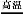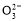题目内容
25 ℃时,浓度为0.2 mol/L的NaHCO3溶液中,下列判断不正确的是( )
A.存在电离平衡HC
 H++C
H++C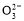
B.存在水解平衡HC +H2O
+H2O H2CO3+OH-
H2CO3+OH-
C.将溶液加热蒸干、灼烧得Na2O2固体
D.加入NaOH固体,恢复到原温度,c(OH-)、c(C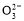 )均增大
)均增大
C
【解析】在水溶液中HC 存在着电离平衡和水解平衡,故A、B正确。将溶液加热蒸干,灼烧后得Na2CO3固体,故C错误。加入NaOH固体,发生反应:HC
存在着电离平衡和水解平衡,故A、B正确。将溶液加热蒸干,灼烧后得Na2CO3固体,故C错误。加入NaOH固体,发生反应:HC +OH-
+OH- C
C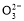 +H2O,所以c(OH-)、c(C
+H2O,所以c(OH-)、c(C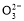 )均增大,D正确。
)均增大,D正确。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目