题目内容
10.下列有关物质分类的说法中,正确的是( )| A. | SiO2不能和水反应,所以它不是酸性氧化物 | |
| B. | 只由一种元素组成的物质必然是纯净物 | |
| C. | 烧碱、冰醋酸、石墨均为电解质 | |
| D. | 海水、氯水、氨水均为混合物 |
分析 A、酸性氧化物能和碱反应生成盐和水,一般溶于水生成碱;
B、同素异形体形成的混合物是一种元素组成;
C、电解质是水溶液中或熔融状态下导电的化合物;
D、混合物是由不同物质组成的.
解答 解:A、SiO2能与碱反应生成盐和水:SiO2+2NaOH=Na2SiO3+H2O,属于酸性氧化物,故A错误;
B、只有一种元素组成的物质可能是混合物,如:氧气和臭氧混合,故B错误;
C、烧碱是氢氧化钠属于电解质、冰醋酸使醋酸是电解质、四氯化碳是非电解质、石墨是单质不是电解质,故C错误;
D、海水是各种盐的水溶液、氯水是氯气的水溶液、氨水为氨气的水溶液,均为混合物,故D正确;
故选D.
点评 本题考查物质的分类,题目较为简单,掌握相关概念即可解答,学习中注意对概念的理解要准确.

练习册系列答案
相关题目
1.下列叙述正确的是( )
| A. | 等质量的铝分别与足量氢氧化钠溶液和稀硝酸反应,放出的氢气一样多 | |
| B. | H2、SO2、CO2三种气体多可用浓硫酸干燥 | |
| C. | 自来水厂常用明矾对水进行消毒杀菌 | |
| D. | 将稀硫酸滴加到Fe(NO3)2溶液中无明显现象 |
18.下列说法错误的是( )
| A. | 乙醇和乙酸都是常用调味品的主要成分 | |
| B. | 乙醇和乙酸都能发生氧化反应 | |
| C. | 乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高 | |
| D. | 乙醇和乙酸分子都含有羟基,都能使酸性高锰酸钾溶液褪色 |
5. 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn( S )+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn( S )+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn( S )+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn( S )+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )| A. | 往平衡体系中加入金属铅后,c(Pb2+)增大 | |
| B. | 往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 | |
| C. | 升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 | |
| D. | 当溶液中固体质量不再变化时达到平衡状态 |
15.下列各组离子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式正确的是( )
| 选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
| A | Fe2+、NO3-、NH4+ | NaHSO4溶液 | 3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
| B | Ca2+、HCO3-、Cl- | 少量NaOH溶液 | Ca2++2HCO3-+2OH-═2H2O+CaCO3↓+CO32- |
| C | K+、AlO2-、HCO3- | 通入少量CO2 | 2AlO2-+3H2O+CO2═2Al(0H)3↓+CO32- |
| D | NH4+、Al3+、SO42- | 少量Ba(OH)2 溶液 | 2 NH4++2SO42-+Ba2++2OH═BaSO42-+2NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
2.目前,工业上冶炼铝通常采用的方法是( )
| A. | 锌置换法 | B. | 铝热反应法 | C. | 氢气置换法 | D. | 电解法 |
19.下列说法正确的是( )
| A. | 溶液是电中性的,胶体则是带电的 | |
| B. | 次氯酸具有强氧化性,属于强电解质 | |
| C. | 铜在氯气中燃烧产生棕色的烟,产物的稀溶液为蓝色 | |
| D. | 铁与稀硝酸充分反应后铁没有剩余,则溶液中一定有Fe3+ |
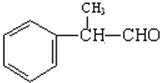 ,请回答以下问题:
,请回答以下问题: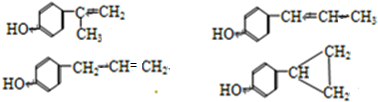
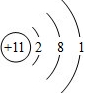 ,YX3的电子式为
,YX3的电子式为 (用元素符号表示).
(用元素符号表示).