题目内容
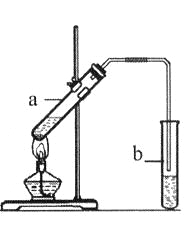
【题目】实验室用燃烧法测定某液有机物A的分子组成,取6.9 g A使之与过量O2燃烧,生成物依次通入足量的浓硫酸和碱石灰,测得浓硫酸增重8.1 g,碱石灰增重13.2 g。又测得A的蒸汽密度是相同条件下氢气密度的23倍,试通过计算来确定A的分子式_____________。
【答案】C2H6O
【解析】
浓硫酸可以吸收水,碱石灰可以吸收二氧化碳,根据原子守恒计算分子中C、H原子数目,进而确定是否含有O元素,确定有机物的分子式。
A的蒸汽密度是相同条件下氢气密度的23倍,由于H2的相对分子质量为2,则有机物A的相对分子质量M=2×23=46,6.9 g该有机物的物质的量n=![]() =0.15 mol,浓硫酸增重8.1 g,则生成水的质量是8.1g,生成n(H2O)=
=0.15 mol,浓硫酸增重8.1 g,则生成水的质量是8.1g,生成n(H2O)=![]() =0.45 mol,其中含有H原子的物质的量n(H)=0.9 mol,碱石灰增重13.2 g,则生成CO2的质量是13.2 g,则n(CO2)=
=0.45 mol,其中含有H原子的物质的量n(H)=0.9 mol,碱石灰增重13.2 g,则生成CO2的质量是13.2 g,则n(CO2)=![]() =0.3 mol,根据C原子守恒可知n(C)=0.3 mol,则m(O)=6.9 g-0.9 mol×1 g/mol-0.3 mol×12 g/mol=2.4 g,所以n(O)=
=0.3 mol,根据C原子守恒可知n(C)=0.3 mol,则m(O)=6.9 g-0.9 mol×1 g/mol-0.3 mol×12 g/mol=2.4 g,所以n(O)=![]() =0.15 mol,n(A):n(C):n(H):n(O)=0.15 mol:0.3 mol:0.9 mol:0.15 mol=1:2:6:1,因此有机物A分子式为:C2H6O。
=0.15 mol,n(A):n(C):n(H):n(O)=0.15 mol:0.3 mol:0.9 mol:0.15 mol=1:2:6:1,因此有机物A分子式为:C2H6O。

【题目】下表为元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | ⑦ | ⑨ | |||||
3 | ① | ③ | ④ | ⑤ | ⑧ | |||
4 | ② |
(1)①~⑨中,最活泼的金属元素是________,最不活泼的元素是______。(写元素符号)。
(2)⑦和⑧的气态氢化物,更稳定的是_____(写电子式)。
(3)原子半径:①_____⑥(填“>
(4)①~⑧的最高价氧化物对应的水化物中:酸性最强的是_____(填化学式,下同);碱性最强的是_______,具有两性的是_______。
(5)①的最高价氧化物对应的水化物与⑧的气态氢化物水溶液发生反应,其离子方程式是___。