题目内容
利用下列装置,可完成很多电化学实验。下列有关叙述,正确的是
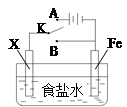

| A.若X为锌棒,开关K置于A处,可减缓铁的腐蚀,这种方法称为牺牲阴极的阳极保护法 |
B.若X为铜棒,开关K置于A处,装置中发生的总反应为2NaCl+2H2O 2NaOH+Cl2↑+H2↑ 2NaOH+Cl2↑+H2↑ |
| C.若X为碳棒,开关K置于B处,在铁棒附近滴入铁氰化钾溶液可看到溶液变血红色 |
| D.若X为碳棒,开关K置于B处,向食盐水中滴入酚酞溶液可看到碳棒附近先变红 |
D
试题分析:A、若X为锌棒,开关K置于A处,则此时构成电解池,铁作阴极可减缓铁的腐蚀,这种方法称为外加电流的阴极保护法,A不正确;B、若X为铜棒,开关K置于A处,则此时构成电解池,铜电极是阳极,失去电子,铁是阴极,装置中不可能发生的总反应为2NaCl+2H2O
 2NaOH+Cl2↑+H2↑,B不正确;C、若X为碳棒,开关K置于B处,则此时构成原电池。铁是负极,失去电子生成亚铁离子,因此在铁棒附近滴入铁氰化钾溶液看不到溶液变血红色,C不正确;D、若X为碳棒,开关K置于B处,则此时构成原电池。铁是负极,碳棒是正极,溶液中的氧气得到电子生成氢氧根离子,因此向食盐水中滴入酚酞溶液可看到碳棒附近先变红,D正确,答案选D。
2NaOH+Cl2↑+H2↑,B不正确;C、若X为碳棒,开关K置于B处,则此时构成原电池。铁是负极,失去电子生成亚铁离子,因此在铁棒附近滴入铁氰化钾溶液看不到溶液变血红色,C不正确;D、若X为碳棒,开关K置于B处,则此时构成原电池。铁是负极,碳棒是正极,溶液中的氧气得到电子生成氢氧根离子,因此向食盐水中滴入酚酞溶液可看到碳棒附近先变红,D正确,答案选D。
练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
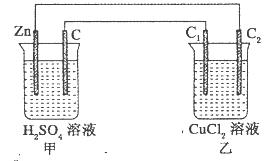
 的酸性废水,最终使铬元素以Cr(OH)3沉淀的形式除去。某科研小组用该原理处理污水,设计装置如图所示。下列说法一定不正确的是( )
的酸性废水,最终使铬元素以Cr(OH)3沉淀的形式除去。某科研小组用该原理处理污水,设计装置如图所示。下列说法一定不正确的是( )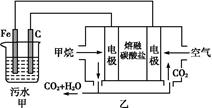
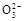
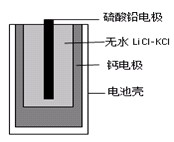
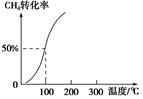
 ,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
,其他条件不变,对平衡体系产生的影响是________(填字母序号)。