题目内容
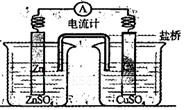
热激活电池可用作火箭、导弹的工作电池。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池的总反应方程式为:PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb。下列有关说法正确的是( )
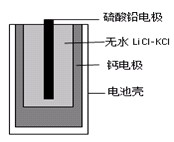
A.常温时,在正负极间接上电流表或检流计,指针不偏转B.放电过程中,Li+向负极移动
C.每转移0.1mol电子,理论上生成20.7gPb
D.正极反应式:Ca +2Cl--2e-=CaCl2

|
C.每转移0.1mol电子,理论上生成20.7gPb
D.正极反应式:Ca +2Cl--2e-=CaCl2
A
试题分析:A、常温时,无水LiCl-KCl呈固态,不会导电,正确;B、在原电池中,阳离子向正极移动,错误;C、铅由+2价降到0价,转移电子2mol。所以生成20.7gPb转移电子0.2mol;D、正极发生的是还原反应。

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目

 MgxMo3S4,下列说法错误的是( )
MgxMo3S4,下列说法错误的是( )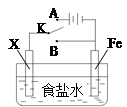
 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑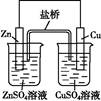
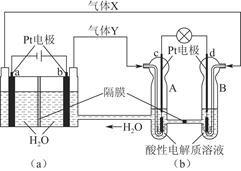
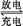 3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )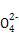 +4H2O+3e-
+4H2O+3e-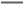 Fe(OH)3+5OH-
Fe(OH)3+5OH-