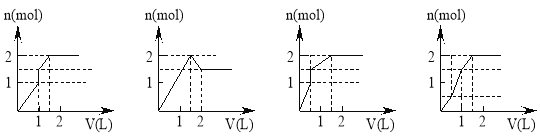��Ŀ����
����Ŀ������Ԫ�����ڱ���һ���֣���֪��Ϊ������Ԫ�أ��䵥��Ϊ����ɫ���壬�ݱ��ش��й����⣺
�� | �� | ||||||
�� | �� | �� | �� | �� | |||
�� | �� |
��1������Ԫ�آ��ԭ�ӽṹʾ��ͼ
��2������ЩԪ���У�����õķǽ���Ԫ���� �� ����õ�Ԫ������дԪ�ط��� ����
��3������ЩԪ�ص�����������Ӧˮ�����У�������ǿ������д��ѧʽ���������Ե�������������д��ѧʽ����д������֮�䷴Ӧ�����ӷ���ʽ��
��4���ڢ�����У���ѧ���ʽϻ��õ�����дԪ�ط��� ����д��������֤�ý��۵�һ����ѧ��Ӧ��ʽ ��
���𰸡�
��1��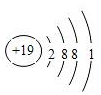
��2��F��Ar
��3��KOH��Al��OH��3��Al��OH��3+OH��=AlO2��+2H2O
��4��Cl��Cl2+2NaBr=Br2+2NaCl
���������⣺��Ϊ������Ԫ�أ��䵥��Ϊ����ɫ���壬���ΪSԪ�أ���Ԫ�ص����λ�ÿ�֪����ΪLi����ΪF����ΪNa����ΪMg����ΪAl����ΪCl����ΪK����ΪBr����1����ΪKԪ�أ�ԭ�Ӻ�����19�����ӣ����������Ϊ2��8��8��1��ԭ�ӽṹʾ��ͼΪ��  �����Դ��ǣ�
�����Դ��ǣ� 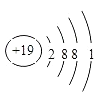 ����2������ЩԪ���У�F�ķǽ�������ǿ��������õķǽ�����F��ϡ��������������ȶ���������õ���Ar�����Դ��ǣ�F��Ar����3��������Խǿ����Ӧ��ļ���Խǿ������ЩԪ�ص�����������Ӧˮ�����У�������ǿ�Ļ�����Ļ�ѧʽ��KOH��������������ǿ�ᡢǿ�Ӧ��������ˮ��������������������������������ط�Ӧ����ƫ����ء�ˮ�����ӷ���ʽΪ��Al��OH��3+OH��=AlO2��+2H2O�����Դ��ǣ�KOH��Al��OH��3��Al��OH��3+OH��=AlO2��+2H2O����4��ͬ������ϵ��£��ǽ����Լ��������ȵķǽ�����ǿ���壬����������������廯�Ƶ�����Һ���û�������֤����Ӧ�ķ���ʽΪ��Cl2+2NaBr=Br2+2NaCl�����Դ��ǣ�Cl��Cl2+2NaBr=Br2+2NaCl��
����2������ЩԪ���У�F�ķǽ�������ǿ��������õķǽ�����F��ϡ��������������ȶ���������õ���Ar�����Դ��ǣ�F��Ar����3��������Խǿ����Ӧ��ļ���Խǿ������ЩԪ�ص�����������Ӧˮ�����У�������ǿ�Ļ�����Ļ�ѧʽ��KOH��������������ǿ�ᡢǿ�Ӧ��������ˮ��������������������������������ط�Ӧ����ƫ����ء�ˮ�����ӷ���ʽΪ��Al��OH��3+OH��=AlO2��+2H2O�����Դ��ǣ�KOH��Al��OH��3��Al��OH��3+OH��=AlO2��+2H2O����4��ͬ������ϵ��£��ǽ����Լ��������ȵķǽ�����ǿ���壬����������������廯�Ƶ�����Һ���û�������֤����Ӧ�ķ���ʽΪ��Cl2+2NaBr=Br2+2NaCl�����Դ��ǣ�Cl��Cl2+2NaBr=Br2+2NaCl��

����Ŀ��ij�о�С����ij2L�ܱ������м���һ�����Ĺ���A������B��������ӦA��s��+2B��g��![]() D��g��+E��g����H=QkJ��mol-1����T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ����ʵ������±���
D��g��+E��g����H=QkJ��mol-1����T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ����ʵ������±���
ʱ�䣨min�� ���ʵ�����mol�� | 0 | 10 | 20 | 30 | 40 | 50 |
B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
��1��T1��ʱ���÷�Ӧ��ƽ�ⳣ��K=_____��
��2��30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬���ݱ��е������жϸı������������____������ĸ��ţ���
a��ͨ��һ������B��������������b������һ�����Ĺ���A
c���ʵ���С�������������������d�����߷�Ӧ��ϵ�¶�
e��ͬʱ����0.2molB��0.1molD��0.1molE
��3��ά��������������¶�T1���䣬����������м���1.60molB��0.20molD��0.20molE��nmolA���ﵽƽ����������20����ʱ�����ʵ�Ũ����ȫ��ͬʱ����Ͷ�����A�����ʵ���nȡֵ��Χ_______��
��4��ά��������������¶�T1���䣬�����ʵ���ʼ���ʵ���Ϊ��n��A��=1.0mol��n��B��=3.0mol��n��D��=amol��n��E��=0mol���ﵽƽ���n��E��=0.50mol����a=_______��
��5�������ܱ��������ȣ�ʵ����B��ת����B%��ʱ��仯��ʾ��ͼ��ͼ��ʾ��ͼ��֪��Q_____0����������������С��������c��v��______v�棨��������������С������������������