题目内容
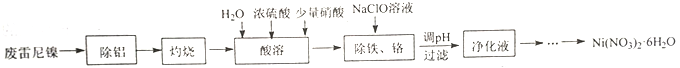
【题目】用废雷尼镍(主要成分为NiO、Al,少量Cr、Fe、C、S及有机物)制备Ni(NO3)2·6H2O的实验流程如下:
已知:①在实验条件下,Ni2+、Cr3+在溶液中不能被NaClO或HNO3氧化。
②NiSO4易溶于水,NiCO3难溶于水;Ni(NO3)2在20℃、90℃时溶解度依次为79.2、188g/100g水。
③己知“酸溶”后的溶液中主要的四种离子开始沉淀与沉淀完全的pH如下:
Ni2+ | Fe2+ | Fe3+ | Cr3+ | |
开始沉淀pH | 6.2 | 7.6 | 2.3 | 4.5 |
沉淀完全pH | 8.5 | 9.1 | 3.3 | 5.6 |
(1)“除铝”所用试剂及主要操作为__________。
(2)“灼烧”的主要目的是__________。
(3)“酸溶”时,用浓硫酸和水代替稀硫酸的目的是__________。
(4)“除铁、铬”时,Fe2+被氧化为Fe3+的离子方程式为__________;氧化后需将溶液pH调整到的范围是__________。
(5)请设计由“净化液”制取Ni(NO3)2·6H2O的实验方案:__________,离心分离、洗涤、干燥得Ni(NO3)2·6H2O (实验中须使用的试剂有:6mol·L-1硝酸,3 mol·L-1Na2CO3溶液)。
【答案】 用NaOH溶液浸泡、过滤、洗涤及干燥 除去C、S及有机物 利用浓硫酸与水混合放热,使溶液温度升高,加快酸溶速率 2Fe2++ClO-+2H+=2Fe3++Cl-+H2O 5.6<pH<6.2 边搅拌边向“净化液”中滴加3mol·L-1Na2CO3溶液至有大量沉淀,静置,向上层清液中滴加3mol·L-1Na2CO3溶液,若无沉淀,过滤,水洗,向滤渣中加入6mol·L-1硝酸至滤渣恰好溶解,蒸发浓缩、冷却结晶
【解析】(1)“除铝”利用铝能与氢氧化钠溶液反应,而其他物质不与氢氧化钠溶液反应,所用试剂及主要操作为用NaOH溶液浸泡、过滤、洗涤及干燥;(2)“灼烧”的主要目的是除去C、S及有机物;(3)“酸溶”时,用浓硫酸和水代替稀硫酸的目的是利用浓硫酸与水混合放热,使溶液温度升高,加快酸溶速率;(4)“除铁、铬”时,Fe2+被次氯酸钠氧化为Fe3+的离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H2O;氧化后需将溶液pH调整使铁离子沉淀完全而铬还没有开始沉淀,则调整到的范围是5.6<pH<6.2;(5)请设计由“净化液”制取Ni(NO3)2·6H2O的实验方案:边搅拌边向“净化液”中滴加3mol·L-1Na2CO3溶液至有大量沉淀,静置,向上层清液中滴加3mol·L-1Na2CO3溶液,若无沉淀,过滤,水洗,向滤渣中加入6mol·L-1硝酸至滤渣恰好溶解,蒸发浓缩、冷却结晶,离心分离、洗涤、干燥得Ni(NO3)2·6H2O。

【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是
选项 | 反应类型 | 反应条件 |
A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
A. A B. B C. C D. D