题目内容
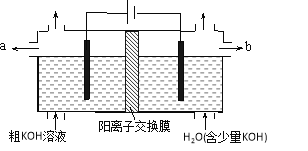
【题目】常温下,向20.00 mL 0.100 0 mol·L-1NH4Cl溶液中逐滴加入0.100 0 mol·L-1KOH溶液时,溶液的pH与KOH溶液体积的关系如图所示(不考虑挥发)。下列说法正确的是( )
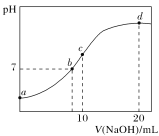
A.点a所示溶液中水的电离程度小于相同温度下纯水的电离程度
B.点b所示溶液中:c(NH4+)=c(K+)=c(H+)=c(OH-)
C.点d所示溶液中的溶质为一水合氨
D.点c所示溶液中:c(K+)+c(H+)=c(NH3·H2O)+c(OH-)
【答案】D
【解析】
A.酸或碱抑制水电离,含有弱离子的盐促进水电离,a点溶质为氯化铵,是强酸弱碱盐,NH4+促进水的电离,则a所示溶液中水的电离程度大于相同温度下纯水的电离程度,A错误;
B.b点溶液呈中性,则c(H+)=c(OH-),水的电离程度很小,盐电离产生的离子浓度大于水电离产生的离子浓度,所以c(K+)>c(H+),B错误;
C.d点KOH溶液体积与NH4Cl溶液的体积相等,二者浓度相等,则二者恰好完全反应,混合溶液中溶质为反应产生的KCl、NH3·H2O等物质的量浓度的混合溶液,C错误;
D.c点溶液中溶质为等物质的量浓度的一水合氨、KCl、NH4Cl的混合溶液,溶液中存在电荷守恒c(NH4+)+c(K+)+c(H+)=c(OH-)+c(Cl-)、同时存在物料守恒:c(NH3H2O)+c(NH4+)= c(Cl-),则c(K+)+c(H+)=c(NH3H2O)+ c(OH-),D正确;
故合理选项是D。

 小题狂做系列答案
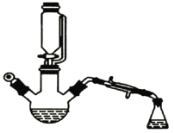
小题狂做系列答案【题目】用下图所示装置制备乙酸乙酯粗产品(加热和夹持装置等省略),有关数据如下表所示:
物质 | C2H5OH | CH3COOH | CH3COOC2H5 |
密度g/cm3 | 0.79 | 1.05 | 0.90 |
沸点/℃ | 78.3 | 118 | 77.1 |
已知:乙醇可以和氯化钙反应生成微溶于水的CaC12·6C2H5OH。在三颈烧瓶内将过量的乙醇和少量的浓硫酸混合,然后经恒压分液斗边滴加酸,边加热蒸馏。得到含有乙醇、醋酸和水的乙酸乙酯粗产品。
(1)混合乙醇与浓硫酸时,应先加入的试剂是_______;浓硫酸的作用是__________。
(2)边滴加醋酸,边加热蒸馏的目的是_______。将粗产品再经下列步骤精制:
(3)为除去其中的醋酸,可向粗产品中加入______(填序号)。
A.无水乙醇 B.碳酸钠粉末 C.无水醋酸钠
(4)向其中加入饱和氯化钙溶液。振荡、分离。其目的是______。
(5)然后再向其中加入无水硫酸钠,振荡,静置,以除去水分。最后,将经过上述处理后的液体放入一干燥的蒸馏烧瓶内。再蒸馏,弃去低沸点馏分,收集沸程76℃~____℃(填“78”或“118“)之间的馏分即得纯净的乙酸乙酯。
(6)在实验中原料用量:23.0mL乙醇、15.0mL冰醋酸,最终得到16.0mL乙酸乙酯,则本次实验中乙酸乙酯的产率为________(百分数精确到0.1)。
【题目】过氧化钙(CaO2)常用作种子及谷物的无毒性消毒剂,常温下为白色的固体,微溶于水,且不溶于乙醇、乙醚和碱性溶液,但溶于酸。某实验小组拟探究CaO2的性质及其实验室制法。
(1)实验探究CaO2与酸的反应。
操作 | 现象 |
向盛有4gCaO2的大试管中加入10mL稀盐酸得溶液a | 剧烈反应,产生能使带火星木条复燃的气体 |
取5mL溶液a置于试管中,滴入两滴石蕊溶液 | 溶液变红,一段时间后溶液颜色明显变浅,稍后溶液变为无色 |
①CaO2与盐酸反应的化学方程式为_____________。
②加入石蕊溶液后溶液褪色可能是因为溶液a中存在较多的_____________。
(2)用如图所示装置制备过氧化钙,其反应原理为Ca+O2![]() CaO2。
CaO2。
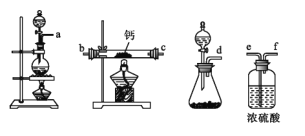
①请选择实验所需要的装置,按气流方向连接的顺序为_____________(填仪器接口的字母,上述装置可不选用也可重复使用)。
②根据完整的实验装置进行实验,实验步骤如下:Ⅰ.检验装置的气密性后,装入药品;Ⅱ.打开分液漏斗活塞,通入气体一段时间,加热药品;Ⅲ.反应结束后,_____________(填操作);Ⅳ.拆除装置,取出产物。
(3)利用反应Ca2++H2O2+2NH3+8H2O=CaO28H2O↓+2![]() 在碱性环境下制取CaO2的装置如图所示。
在碱性环境下制取CaO2的装置如图所示。
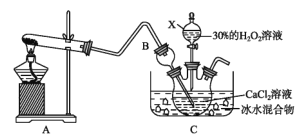
①NH3在Ca2+和H2O2的反应过程中所起的作用是_____________。
②反应结束后,经过滤、洗涤、低温烘干可获得CaO28H2O。过滤需要的玻璃仪器是_____________;将沉淀进行洗涤的操作为_____________。