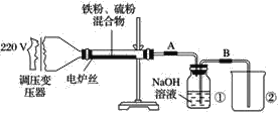
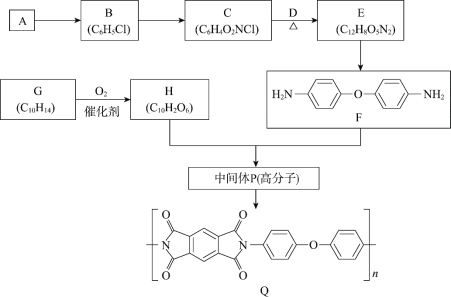
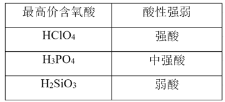
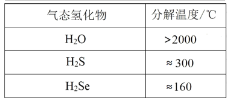
��Ŀ����
����Ŀ����Cl-Ũ��Ϊ0.5 mol��L��1��ij��ɫ������Һ�У������ܺ����±��е����������ӡ�
������ | K�� ��Ag���� Mg2�� ��Ba2�� Fe3+ |
������ | NO3-�� CO32- ��SiO32- ��SO42- |
��ʾ��SiO32-��2H��=H2SiO3��(H2SiO3�ǰ�ɫ����)��H2SiO3![]() SiO2��H2O
SiO2��H2O
��ȡ����Һ100 mL��������ʵ��(����������ڱ�״���²ⶨ)��
��� | ʵ������ | ʵ���� |
�� | �����Һ�м�������ϡ���� | ������ɫ�������ų���״����0.56 L���� |
�� | ����ķ�Ӧ���Һ���ˣ��Գ���ϴ�ӡ����������أ��������ù������� | ��������Ϊ2.4 g |
�� | ������Һ�еμ�BaCl2��Һ | ���������� |
��ش��������⡣
(1)ͨ������ʵ����ȷ��һ�������ڵ���������______��һ�������ڵ���������________��
(2)ͨ��ʵ���ͱ�Ҫ���㣬��д��һ�����ڵ������Ӽ���Ũ��(��һ��Ҫ����)
������ | ��___ | ��___ | ||
c/mol��L��1 | ____ | ___ |
(3)�ж�K���Ƿ���ڣ�������������СŨ�ȣ���������˵�����ɣ�_______________��
���𰸡�Ag����Mg2����Ba2����Fe3+ SO42- CO32- SiO32- 0.25 0.4 ���ڣ���СŨ��Ϊ1.8mol��L��1
��������
������֪��ҺΪ��ɫ������Һ��һ������Fe3+������Һ�к��е����ӱ����ܴ������森��ʵ����֪������Һ��һ������CO32-����Ũ��Ϊ![]() ==0.25mol/L����һ��û��Ag+��Mg2+��Ba2+�������ɰ�ɫ�����ж���Һ��һ������SiO32-��������ӦSiO32-+2H+=H2SiO3����SiO32-��Ũ��Ϊ
==0.25mol/L����һ��û��Ag+��Mg2+��Ba2+�������ɰ�ɫ�����ж���Һ��һ������SiO32-��������ӦSiO32-+2H+=H2SiO3����SiO32-��Ũ��Ϊ![]() ==0.4mol/L����ʵ����֪��Һ�в���SO42-�����ݵ���غ�2c��CO32-��+2c��SiO32-��+c��Cl-��=2��0.25mol/L+2��0.4mol/L+0.5molL-1=1.8mol/L�������Һ��һ������K+������Ũ������Ϊ1.8mol/L������ȷ��NO3-�Ƿ���ڣ��Դ������
==0.4mol/L����ʵ����֪��Һ�в���SO42-�����ݵ���غ�2c��CO32-��+2c��SiO32-��+c��Cl-��=2��0.25mol/L+2��0.4mol/L+0.5molL-1=1.8mol/L�������Һ��һ������K+������Ũ������Ϊ1.8mol/L������ȷ��NO3-�Ƿ���ڣ��Դ������
��1��(1)ͨ������ʵ����ȷ��һ�������ڵ���������Ag����Mg2����Ba2����Fe3+��һ�������ڵ���������SO42-��
�𰸣�Ag����Mg2����Ba2����Fe3+ SO42-
��2��������������֪��c��CO32-��=0.25mol/L��c��SiO32-��=0.4mol/L��
�𰸣�CO32- SiO32- 0.25 0.4
��3����2c��CO32-��+2c��SiO32-��+c��Cl-��=2��0.25mol/L+2��0.4mol/L+0.5molL-1=1.8mol/L�����ݵ���غ��֪��Һ��һ������K+������Ũ������Ϊ1.8mol/L��
�𰸣����ڣ���СŨ��Ϊ1.8mol��L��1

 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
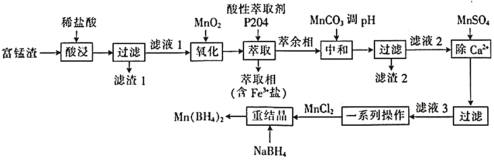
����ѵ��ϵ�д�����Ŀ�����⻯��![]() ��������������ϣ�Ҳ�����ڿ�ѧ�о����Ը�����(��60% MnO��������SiO2��Al2O3��CaO��FeO)Ϊԭ���Ʊ����⻯�̵Ĺ����������¡�
��������������ϣ�Ҳ�����ڿ�ѧ�о����Ը�����(��60% MnO��������SiO2��Al2O3��CaO��FeO)Ϊԭ���Ʊ����⻯�̵Ĺ����������¡�
��֪�������������Ksp ��ֵ���±���
�������� |
|
|
|
|
Ksp |
|
|
|
|
��ش��������⣺
(1) NaBH4��B�Ļ��ϼ�Ϊ________�ۡ�
(2)����������������1��������Ӧ(���»�����)����________(����ĸ)��
A��Ũ���� B������������Һ C��̼���� D�������
(3)���������з�����Ӧ�����ӷ���ʽΪ________________���÷�Ӧ�������ԣ�![]() ________(�
________(�![]() ����
����![]() ��) MnO2��
��) MnO2��
(4)���к͡�ʱ������pHԼΪ________��(����Һ�е�����Ũ��С��![]() ʱ�������ﵽ��ȫ���������2λ��Ч����)
ʱ�������ﵽ��ȫ���������2λ��Ч����)
(5) Mn(BH4)2����ϡ���ᷴӦ����H3BO3���÷�Ӧ�Ļ�ѧ����ʽΪ________________��
(6)�ⶨ�����������ĺ�����ȡ20g����������������������������ˡ�������������ȡ������ȡ��(����Fe3+span>ȫ������ȡ)ת���ձ��У���������ϡ���ᣬ��ַ�Ӧ���á���Һ������Fe3+����Һ�м�������KI����ַ�Ӧ����Һ���Ƴ�500mL��ȡ25mL����ƿ�в��������ָʾ���������![]() ��Na2S2O3��Һ�ζ�����������ƽ��ʵ�飬�������Na2S2O3��Һ����������ʾ��
��Na2S2O3��Һ�ζ�����������ƽ��ʵ�飬�������Na2S2O3��Һ����������ʾ��
ʵ����� | 1 | 2 | 3 |
Na2S2O3��Һ���/ | 23.20 | 24.80 | 25.20 |
��֪��I2+2Na2S2O3==2NaI+Na2S4O6
�ٵζ��ﵽ�յ�ʱ��Һ����ɫ�仯Ϊ________��
�ڸ����������ĺ���Ϊ________��
����Ŀ���״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ��һ������������ַ�Ӧ�ϳɼ״���
��Ӧ��CO(g)+2H2(g) ![]() CH3OH(g)����H1
CH3OH(g)����H1
��Ӧ��C02(g)+3H2(g) ![]() CH30H(g)+ H2O(g)����H2
CH30H(g)+ H2O(g)����H2
�±����������Ƿ�ӦI�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)��
�¶� | 250�� | 300�� | 350�� |
K | 2.O | 0.27 | 0.012 |
��1���ɱ��������ж���H1_____0(�>������<����=��)��Ӧ��C02(g)+H2(g)![]() CO(g)+H20(g) ��H3=____(����H1����H2��ʾ)��
CO(g)+H20(g) ��H3=____(����H1����H2��ʾ)��
��2���������ݻ����䣬���д�ʩ����߷�Ӧ����COת���ʵ���_________(ѡ��ĸ)��
a������CO��ʹ��ϵ��ѹǿ����
b����CH3OH(g)����ϵ�з���
e������He��ʹ��ϵ��ѹǿ����
d��ʹ�ø�Ч����
��3��д����Ӧ��Ļ�ѧƽ�ⳣ������ʽ��K=_________�����ֺ��º��ݵ������½���Ӧ���ƽ����ϵ������Ũ�Ⱦ�����һ������ѧƽ��_________(�������������)�ƶ���ƽ�ⳣ��K____(��������С�����䡱)��