题目内容
【题目】下列数据或事实所呈现的规律不能用元素周期律解释的是
A. B.
B.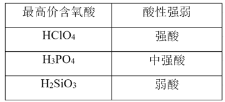
C.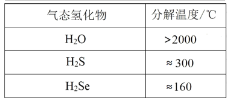 D.
D.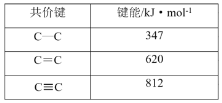
【答案】D
【解析】
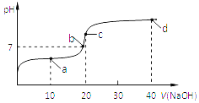
A.F、Cl、Br为同主族元素,核电荷数越大,非金属性越弱,生成的HX越不稳定,生成HX的反应程度越小,故A不选;
B.Si、P、Cl为同周期主族元素,核电荷数越大,非金属性越强,其最高价氧化物水化物的酸性越强,则HClO4酸性最强,故B不选;
C.O、S、Se为同主族元素,核电荷数越大,非金属性越弱,生成的简单氢化物越不稳定,即H2O最稳定,H2Se最不稳定,故C不选;
D.碳碳单键键长最长,键能最小,而碳碳叁键键长最短,键能最大,但键能不是碳碳单键键能的三倍,也不是碳碳单键键能与碳碳双键键能和,与元素周期律无关,故D选;
故答案为D。

 寒假学与练系列答案
寒假学与练系列答案【题目】在Cl-浓度为0.5 mol·L-1的某无色澄清溶液中,还可能含有下表中的若干种离子。
阳离子 | K+ Ag+ Mg2+ Ba2+ Fe3+ |
阴离子 | NO3- CO32- SiO32- SO42- |
提示:SiO32-+2H+=H2SiO3↓(H2SiO3是白色沉淀)、H2SiO3![]() SiO2+H2O
SiO2+H2O
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色沉淀并放出标准状况下0.56 L气体 |
Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4 g |
Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
请回答下列问题。
(1)通过以上实验能确定一定不存在的阳离子是______,一定不存在的阴离子是________。
(2)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,请写出一定存在的阴离子及其浓度(不一定要填满)
阴离子 | ①___ | ②___ | ||
c/mol·L-1 | ____ | ___ |
(3)判断K+是否存在,若存在求其最小浓度,若不存在说明理由:_______________。
【题目】高温下CO2和H2S发生如下反应:CO2(g) +H2S(g)COS(g) +H2O(g)。有关实验数据如下:
实验 | 温度 | 物质的起始物质的量/(mol) | 平衡时COS物质的量/(mol) | |
n(CO2) | n(H2S) | n(COS) | ||
I | 337℃ | 0.10 | 0.40 | 0.01 |
II | 347℃ | 0.10 | 0.40 | 0.015 |
下列说法不正确的是
A.该反应为吸热反应
B.实验I达平衡后COS的物质的量分数为5%
C.实验I温度下,反应的平衡常数为![]()
D.平衡后向II中再充入0.10 mol CO2和0.40 mol H2S,相同温度下再达平衡时n(COS)=0.03mol