题目内容
7.为除去括号内杂质,下列有关试剂和操作方法不正确的是( )| A. | 溴苯(苯):蒸馏 | B. | 乙醇(乙酸):KOH溶液,分液 | ||
| C. | 乙烷(乙烯):溴水,洗气 | D. | 苯(溴):稀NaOH溶液,分液 |
分析 A.二者互溶,但沸点不同;
B.乙酸与KOH反应后,增大与乙醇沸点差异;
C.乙烯与溴水反应,而乙烷不能;
D.溴与NaOH溶液反应后,与苯分层.
解答 解:A.二者互溶,但沸点不同,则蒸馏可分离,故A正确;
B.乙酸与KOH反应后,增大与乙醇沸点差异,然后蒸馏可分离,不能分液,故B错误;
C.乙烯与溴水反应,而乙烷不能,然后洗气可除杂,故C正确;
D.溴与NaOH溶液反应后,与苯分层,然后分液可除杂,故D正确;
故选B.
点评 本题考查混合物的分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
17.请将下列实验错误操作可能会引起的不良后果填在表格中.
| 实验 | 向试管中加锌粒 | 对量筒中液体读数 | 浓H2SO4 |
错误操作 |  |  |  |
不良后果 |
18.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 质量为16g的O2和O3的混合气体中所含的氧原子的个数为NA | |
| B. | 18gNH4+含有质子数为10NA | |
| C. | 1mol过氧化钠与足量水反应时,转移电子的数目为2NA | |
| D. | 标准状况下,相同体积的O2、HCl、H2O含有的分子数相同 |
15.研究PM 2.5、SO2、NOx等,对监测空气质量具有重要意义.取某样本用蒸馏水处理制成待测液,其中所含离子的化学组分及其浓度如下表:
请回答下列问题:
(1)NO3-中心原子的杂化类型是sp2,离子中所含大π键是π46.
(2)根据表中数据计算此待测液中c(H+)浓度a为1×10-4mol/L.
(3)NOx是汽车尾气中的主要污染物之一.
①NOx能形成酸雨,由NO2形成的酸雨中含有的主要离子有H+、NO3-.
②汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是N2+O2═2NO,在汽车尾气系统中加装催化转化器可减少NOx的污染.
(4)为减少SO2的排放,常采取的措施有:
①在燃煤中加入生石灰可以起到固硫的作用,SO2被吸收后转化成一种硫元素的最高价态的化合物,该物质的化学式是CaSO4.
②吸收烟气中的SO2,以下物质可作吸收剂的是a(填序号),写出吸收SO2过程中发生的一个反应的离子方程式2OH-+SO2═SO32-+H2O或OH-+SO2═HSO3-.
a.NaOH b.H2SO4 c.NaHSO3.
| 离子 | K+ | Na+ | NH4+ | H+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | a | 4×10-5 | 3×10-5 | 2×10-5 |
(1)NO3-中心原子的杂化类型是sp2,离子中所含大π键是π46.
(2)根据表中数据计算此待测液中c(H+)浓度a为1×10-4mol/L.
(3)NOx是汽车尾气中的主要污染物之一.
①NOx能形成酸雨,由NO2形成的酸雨中含有的主要离子有H+、NO3-.
②汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是N2+O2═2NO,在汽车尾气系统中加装催化转化器可减少NOx的污染.
(4)为减少SO2的排放,常采取的措施有:
①在燃煤中加入生石灰可以起到固硫的作用,SO2被吸收后转化成一种硫元素的最高价态的化合物,该物质的化学式是CaSO4.
②吸收烟气中的SO2,以下物质可作吸收剂的是a(填序号),写出吸收SO2过程中发生的一个反应的离子方程式2OH-+SO2═SO32-+H2O或OH-+SO2═HSO3-.
a.NaOH b.H2SO4 c.NaHSO3.
2.既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的少量乙烯的操作方法是( )
| A. | 与足量高锰酸钾酸性溶液反应 | B. | 与足量溴水反应 | ||
| C. | 在一定条件下通入氢气 | D. | 分别进行燃烧 |
19.对于A2+3B2═2C的反应,在不同条件下的化学反应速率表示中,反应速率最快的是( )
| A. | v(A2)=0.4mol/(L•s) | B. | v(B2)=0.8mol/(L•s) | ||
| C. | v(C)=0.6mol/(L•s) | D. | v(B2)=5.4mol/(L•min) |
16.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4LNO与0.5molO2充分反应,最后得到NA个NO2分子 | |
| B. | 1.0L 0.5mol/L的NaAlO2水溶液中含有氧原子数为NA | |
| C. | 0.6gCaCO3与Mg3N2的混合物中所含质子数为0.3NA | |
| D. | 某密闭容器盛有0.2molSO2和0.1molO2,在一定条件下充分反应,转移电子的数目为0.4NA |
17.常温下,某溶液中水的电离度a=10-10/55.5(%),该溶液的pH可能是( )
| A. | 12 | B. | 10 | C. | 4 | D. | 3 |

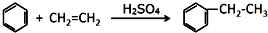
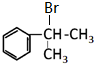 .
.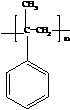 .
. ;
; ,其一氯代物有4种.
,其一氯代物有4种.