题目内容
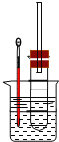
【题目】碳酸亚铁可用于治疗缺铁性贫血。实验室里先制得硫酸亚铁,后将硫酸亚铁与碳酸氢钠反应制得碳酸亚铁(FeSO4+2NaHCO3![]() Na2SO4+FeCO3↓+CO2↑+H2O)。实验装置如下图所示(部分夹持仪器略去)。
Na2SO4+FeCO3↓+CO2↑+H2O)。实验装置如下图所示(部分夹持仪器略去)。
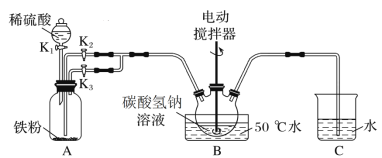
回答下列问题:
(1)A装置中发生反应的化学方程式是________。
(2)实验过程中,将生成的FeSO4溶液和NaHCO3溶液混合的操作是________。
(3)装置B发生反应生成FeCO3的离子方程式是______。
(4)碳酸亚铁在潮湿的空气中逐渐被氧化生成氢氧化铁和一种气体,反应的化学方程式为_________。
(5)配制溶液所用的蒸馏水必须先除去溶解的氧气,具体方法是_______。
(6)设计实验检验制得的产品中是否含Fe3+:________。
【答案】Fe + H2SO4=FeSO4 + H2↑ 关闭K3,打开K2 Fe2++ 2HCO3-=FeCO3↓+ CO2↑+ H2O 4FeCO3 + O2+ 6H2O = 4Fe(OH)3 + 4CO2 将蒸馏水煮沸后迅速冷却 取少量产品放入试管中,加入稀硫酸(或稀盐酸)溶解,再滴入KSCN溶液,若溶液不变为红色,则说明产品中不含Fe3+;若溶液变为红色,则含有Fe3+
【解析】
打开活塞K1、K3,A中稀硫酸和Fe反应生成硫酸亚铁和氢气,关闭K1、K3打开K2,通过气体压强使硫酸亚铁溶液进入B装置,B装置中发生反应![]() ,生成的二氧化碳及A中的氢气通过C检验。
,生成的二氧化碳及A中的氢气通过C检验。
(1)稀硫酸和Fe反应生成硫酸亚铁和氢气;
(2)关闭K1、K3打开K2通过气体压强使硫酸亚铁溶液进入B装置;
(3) B装置中发生反应![]() ;
;
(4)碳酸亚铁在潮湿的空气中逐渐被氧化生成氢氧化铁和一种气体,根据元素守恒确定生成气体成分;
(5) 氧气在蒸馏水中的溶解度随着温度的升高而降低;
(6)用KSCN溶液鉴别溶液中是否含有Fe3+。
打开活塞K1、K3,A中稀硫酸和Fe反应生成硫酸亚铁和氢气,关闭K1、K3打开K2,通过气体压强使硫酸亚铁溶液进入B装置,B装置中发生反应![]() ,生成的二氧化碳及A中的氢气通过C检验。
,生成的二氧化碳及A中的氢气通过C检验。
(1)A装置中发生反应的化学方程式:![]() ,故答案为:
,故答案为:![]() ;
;
(2)实验过程中,将生成的FeSO4溶液和NaHCO3溶液混合的操作是关闭K1、K3打开K2通过气体压强使硫酸亚铁溶液进入B装置,故答案为:关闭K3,打开K2;
(3)B装置中发生反应![]() ,故答案为:
,故答案为:![]() ;
;
(4)碳酸亚铁在潮湿的空气中逐渐被氧化生成氢氧化铁和一种气体,根据元素守恒确定生成气体成分为二氧化碳,反应方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(5)氧气在蒸馏水中的溶解度随着温度的升高而降低,所以配制溶液所用的蒸馏水必须先除去溶解的氧气,具体方法是将蒸馏水煮沸后迅速冷却,故答案为:将蒸馏水煮沸后迅速冷却;
(6)设计实验检验制得的产品中是否含Fe3+,可利用KSCN溶液鉴别,具体操作为:取少量产品放入试管中,加入稀硫酸(或稀盐酸)溶解,再滴入KSCN溶液,若溶液不变为红色,则说明产品中不含Fe3+;若溶液变为红色,则含有Fe3+,故答案为:取少量产品放入试管中,加入稀硫酸(或稀盐酸)溶解,再滴入KSCN溶液,若溶液不变为红色,则说明产品中不含Fe3+;若溶液变为红色,则含有Fe3+。

【题目】满足下列条件的有机物的种类数正确的是
选项 | 有机物 | 条件 | 种类数 |
A | C5H10O2 | 在酸性条件下会水解生成甲和乙,且甲、乙的相对分子质量相等 | 4 |
B | C6H12O2 | 能与 NaHCO3溶液反应 | 3 |
C | C5H12O | 含有2个甲基的醇 | 5 |
D |
| 该有机物的一氯代物 | 4 |
A.AB.BC.CD.D
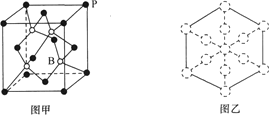
【题目】已知Fe2O3 (s)+3CO(g) ![]() 2Fe(s) +3CO2 (g),则反应达平衡后甲、乙两容器中说法不正确的是( )
2Fe(s) +3CO2 (g),则反应达平衡后甲、乙两容器中说法不正确的是( )
起 始 量 | 温度T℃ 平衡常数K=64 恒容且V=1L | ||||
Fe2O3 | CO | Fe | CO2 | ||
甲 | 1 mol | 1 mol | 1 mol | 1 mol | |
乙 | 1 mol | 2 mol | 1 mol | 1mol | |
A.容器中混合气体的平均相对分子质量不变时反应达平衡
B.乙中CO2的体积分数为50%
C.甲中CO的转化率为60%
D.甲、乙两容器中 CO的体积分数相等