题目内容
【题目】在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是( )
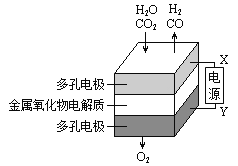
A.阴、阳两极生成的气体的物质的量之比是1︰2
B.X是电源的负极
C.阴极的反应式是:H2O+2e-=H2+O2- CO2+2e-=CO+O2-
D.总反应可表示为:H2O+CO2![]() H2+CO+O2
H2+CO+O2
【答案】A
【解析】
A.从总反应方程式可知,阴极生成2mol气体(H2、CO各1mol)、阳极生成1mol气体(氧气),所以阴、阳两极生成的气体物质的量之比2∶1,故A错误;
B.从图示可看出,与X相连的电极发生H2O→H2、CO2→CO的转化,均得电子,应为电解池的阴极,则X为电源的负极,故B正确;
C.阴极H2O→H2、CO2→CO均得电子发生还原反应,电极反应式分别为:H2O+2eˉ=H2↑+O2ˉ、CO2+2eˉ=CO+O2ˉ,故C正确;
D.从图示可知,阳极生成H2和CO的同时,阴极有O2生成,所以总反应可表示为:H2O+CO2![]() H2+CO+O2,故D正确。
H2+CO+O2,故D正确。
综上所述,答案为A。

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案
相关题目